卵巢低储备(diminished ovarian reserve, DOR)表现为卵巢产生卵子的能力减弱,卵子数量和质量双重下降[1]。研究表明[2],约10%的育龄期妇女经历卵巢储备功能下降而寻求不孕症治疗。目前辅助生殖技术(assisted reproductive technology,ART) 是DOR不孕症患者最有效的治疗方式。促排卵是ART治疗的首要步骤,但DOR患者在接受传统促排卵方案中,表现为对外源性促性腺激素(gonadotropin, Gn) 刺激反应低下,周期取消率升高,获卵数、可用胚胎数减少及妊娠率低下[3-5]。因此,选择合适的促排卵方案是DOR患者接受ART治疗首要考虑的问题。
枸橼酸氯米芬(clomiphene citrate, CC,克罗米芬)为雌激素受体拮抗剂,通过竞争结合下丘脑细胞内的雌激素受体,刺激促卵泡生成素(follicle stimulating hormone,FSH) 和促黄体生成素(luteinizing hormone, LH)的分泌,从而使卵巢内的卵泡生长、发育[6]。Teramoto等[7]的研究发现CC微刺激方案可以使年龄高达45岁的妇女在1个取卵周期至少获得1枚成熟卵子,提高了DOR患者的治疗效率。然而在DOR患者中使用CC微刺激方案促排卵常会引起早发LH峰的出现,导致提前排卵,降低促排卵效率[8]。
高孕激素促排卵方案(progestin-primed ovarian stimulation, PPOS) 是基于全胚冷冻的治疗策略,利用孕激素(外源性或内源性)的负反馈机制阻止促排卵过程中早发LH峰的出现[9-13]。基于卵巢低反应患者的研究[14]发现,PPOS方案较自然周期能有效地抑制过早LH峰的发生及提前排卵,卵泡生长时间更长,且取卵前卵泡的直径更大,可控性增加;实验室结局显示PPOS方案组的获卵数和有效胚胎数较自然周期明显增多,但妊娠结局两组无差异。
因此,本研究进一步回顾性分析近10年我中心应用PPOS方案与CC微刺激方案治疗DOR患者的取卵周期结局及内分泌变化特点,以进一步证实PPOS方案在DOR患者促排卵周期中的可控性,为临床应用提供参考。
1 资料与方法 1.1 研究对象回顾性分析2011年1月至2020年12月因DOR就诊于上海交通大学医学院附属第九人民医院,接受体外受精-胚胎移植(in vitro fertilization-embryo transfer, IVF-ET) 治疗的不孕症患者。
纳入标准[14]:符合不孕症诊断标准,即夫妻双方正常性生活,未避孕1年未孕;年龄25~45岁;双侧卵巢的基础窦卵泡数(antral follicle count,AFC)少于5枚;基础FSH 10~30 U/L; 抗苗勒管激素(anti-Müllerian hormone, AMH) < 1.1 ng/mL;规律自发的月经周期21~35 d。排除标准:月经第3天的雌激素(estrogen, E2)>70 pg/mL;染色体异常,生殖器官畸形和生殖系统肿瘤;患有其他全身性的急慢性疾病。
1.2 促排卵方案PPOS方案:从月经第3天起口服醋酸甲羟孕酮(medroxyprogesterone acetate, MPA, 浙江仙琚制药,2 mg/粒)10 mg,或MPA 10 mg+乙炔雌二醇(ethinyl estradiol,EE,信宜制药,12.5 μg/粒)12.5~25 μg。用药5~7 d后复诊,当卵泡开始生长,同时伴随E2的上升,且FSH < 8.0 U/L时,给予小剂量人尿促性素(human menopausal gonadotropin, hMG;上海丽珠制药有限公司,75 U/支) 75~150 U促进卵泡发育。之后每隔2~4 d进行1次经阴道超声检查以记录发育卵泡大小及数量,并同时测定血清FSH、LH、E2及孕激素(progesterone, P) 浓度,根据卵巢反应情况调整hMG用量。当主卵泡直径≥18 mm时,同时停用MPA和hMG,注射人绒毛膜促性腺激素(human chorionic gonadotropin,hCG,丽珠医药)1 000 U和短效促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonist,GnRH-a,达必佳,德国辉凌)0.1 mg共同诱发排卵。
CC微刺激促排卵方案:从月经第3天起口服CC(塞浦路斯高特制药, 50 mg/粒) 50 mg/d; 3~5 d后复诊,进行经阴道超声检查以记录发育卵泡大小及数量,并同时测定血清FSH、LH、E2、P的浓度。若有1个卵泡的直径大于13 mm,或血清LH较基础值升高1倍以上时,加注促性腺激素释放激素拮抗剂(gonadotropin-releasing hormone antagonist,GnRH-anti,思则凯,默克雪兰诺;0.25 mg/支) 0.125~0.25 mg。根据卵巢反应情况决定是否需要注射hMG (75~150 U) 隔日1次。当主卵泡直径≥18 mm时,注射GnRH-a 0.1 mg诱发排卵。
1.3 取卵及胚胎评估常规在诱发排卵后34~36 h经阴道穿刺取卵。有早发LH峰的出现(LH>20 U/L)时,则于出峰后18~30 h取卵[14]。取卵后按常规进行IVF或卵泡浆内单精子注射(ICSI),胚胎评级按本中心标准评估。
根据胚胎原核评分、发育速度及形态学等参数,卵裂球的大小、形态、数目、胞质情况、碎片的比例进行质量评分,分为4级[15]。Ⅰ级:胚胎卵裂球大小均匀,形态规则且胞质均匀清晰,碎片无或少于10%;Ⅱ级:胚胎卵裂球不等,且形态欠规则, 碎片10%~25%;Ⅲ级:胚胎卵裂球大小不均等,碎片25%~50%;Ⅳ级:胚胎卵裂球大小严重不均,碎片大于50%。Ⅰ级和Ⅱ级胚胎定义为优质胚胎。对优质胚胎进行玻璃化冷冻保存,剩余未达到优质胚胎标准的胚胎予以继续培养,至囊胚形成后冷冻。
1.4 观察及评价指标主要观察指标为早发LH峰比例,次要观察指标包括获卵数(率)、成熟卵数(率)、受精卵数(率)、卵裂数、优质胚胎数、有效胚胎数、促排卵过程中的Gn用量及用药时间和激素水平变化等。
1.5 统计学处理采用RStudio (version 1.3.1093) 建立倾向评分匹配(propensity score matching, PSM)模型,平衡两组基线特征的差异。选择11个协变量通过logistic回归来估计倾向评分,包括年龄、不孕年限、既往移植失败次数、既往无可用胚胎周期次数、体质量指数(body mass index, BMI)及AFC、AMH、FSH、LH、E2、P的基础水平。两组患者采用最近邻随机匹配算法,比例为1∶1。
采用SPSS 25.0统计软件进行统计学分析。计量资料以x±s表示, 计数资料以n(%)表示。正态分布的计量资料采用两个独立样本的t检验;非正态分布的计量资料采用Mann-Whitney U检验;计数资料选用卡方检验进行分析。检验水准(α)为0.05。
2 结果 2.1 两组患者的一般资料共纳入1 827例DOR不孕症患者,匹配后共972例患者,每组486例。结果(表 1)表明:两组患者的年龄、不孕年限、既往移植失败周期及无可用胚胎周期次数、BMI、AMH、AFC以及基础激素水平差异均无统计学意义。
| N=486 | |||||||||||||||||||||||||||||
| 项目 | PPOS组 | CC组 | P | ||||||||||||||||||||||||||
| 年龄/岁 | 40.14±3.72 | 40.25±3.43 | 0.629 | ||||||||||||||||||||||||||
| 不孕年限 | 4.31±2.96 | 4.35±2.79 | 0.791 | ||||||||||||||||||||||||||
| 既往移植失败周期n | 0.6±1.27 | 0.59±1.15 | 0.832 | ||||||||||||||||||||||||||
| 既往无可用胚胎周期n | 0.43±1.07 | 0.57±1.17 | 0.052 | ||||||||||||||||||||||||||
| 体质量指数(kg·m-2) | 21.53±2.66 | 21.38±2.71 | 0.374 | ||||||||||||||||||||||||||
| AMH/(ng·mL-1) | 0.69±0.75 | 0.59±0.55 | 0.512 | ||||||||||||||||||||||||||
| 窦卵泡数/个 | 2.52±1.39 | 2.47±1.50 | 0.594 | ||||||||||||||||||||||||||
| FSH/(U·L-1) | 13.16±2.86 | 13.27±3.42 | 0.583 | ||||||||||||||||||||||||||
| LH/(U·L-1) | 4.33±1.90 | 4.33±2.06 | 0.981 | ||||||||||||||||||||||||||
| E2/(pg·mL-1) | 31.56±16.58 | 32.25±15.25 | 0.499 | ||||||||||||||||||||||||||
| P/(ng·mL-1) | 0.33±0.31 | 0.32±0.39 | 0.714 | ||||||||||||||||||||||||||
结果(表 2)表明:治疗周期结束后,PPOS组的hMG应用天数及剂量明显多于CC组,差异均有统计学意义(P < 0.001)。但CC组中早发LH峰比例(39.92%)显著高于PPOS组(6.17%),差异有统计学意义(P < 0.001),且其诱发排卵至取卵时间较PPOS组明显缩短P < 0.001)。
| N=486 | |||||||||||||||||||||||||||||
| 观察指标 | PPOS组 | CC组 | P值 | ||||||||||||||||||||||||||
| hMG应用天数 | 7.35±3.17 | 3.11±3.19 | < 0.001 | ||||||||||||||||||||||||||
| hMG剂量/U | 1 098.46±606.55 | 463.89±541.15 | < 0.001 | ||||||||||||||||||||||||||
| 诱发排卵至取卵时间/h | 34.21±7.60 | 25.54±14.82 | < 0.001 | ||||||||||||||||||||||||||
| 早发LH峰n(%) | 30(6.17) | 194(39.92) | < 0.001 | ||||||||||||||||||||||||||
| 周期取消率n(%) | 0(0.00) | 5(1.03) | 0.463 | ||||||||||||||||||||||||||
| 周期取消率:无有效胚胎的周期数/总取卵周期数×100% | |||||||||||||||||||||||||||||
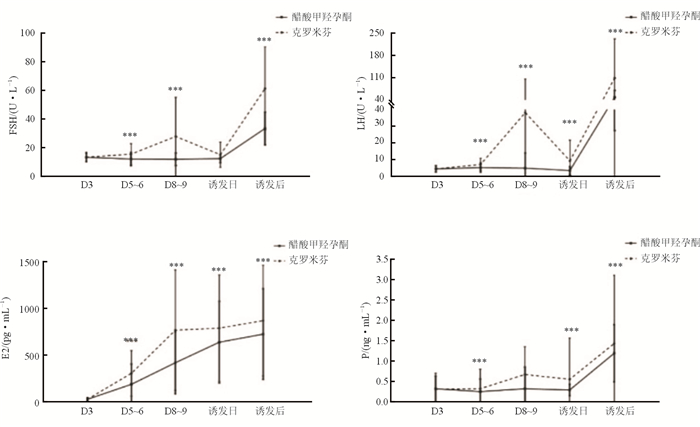
结果(图 1)表明:PPOS组与CC组患者基础FSH均高于10 U/L[(13.16±2.86) U/L vs (13.27±3.42) U/L]。促排卵过程中,PPOS组FSH (D3: 13.16 U/L; D 5~6: 11.94 U/L; D8~9: 11.77 U/L)和LH[D3: (4.33±1.90) U/L;D5~6: (5.12±2.76) U/L;D8~9: (4.79±9.07) U/L]水平呈现平稳状态。而在CC组中,随着促排卵时间的延长,FSH和LH均呈明显升高趋势,特别是LH水平,在促排卵后期较基础水平明显升高(38.01 U/L vs 4.33 U/L, P < 0.001)。与FSH和LH相应,CC组患者E2及P水平也较PPOS组偏高(P < 0.001)。
|
| 图 1 促排卵过程中各时间点激素变化 ***P < 0.001 |
结果(表 3)表明:两组患者获卵数(率)、成熟卵数、正常受精卵数(率)、卵裂数、有效胚胎数及卵子利用率差异均无统计学意义。但PPOS方案组患者成熟卵率明显高于CC组(0.87±0.29 vs 0.78±0.35, P < 0.001),可能与PPOS方案相对容易控制取卵时间相关。
| 观察指标 | PPOS组(N=101) | CC组(N=99) | P值 |
| 获卵数 | 1.81±1.33 | 2.00±1.69 | 0.061 |
| 获卵率/% | 73±34 | 71±31 | 0.423 |
| 成熟卵数 | 1.58±1.25 | 1.54±1.36 | 0.590 |
| 成熟卵率/% | 87±29 | 78±35 | < 0.001 |
| 正常受精卵数 | 1.27±1.16 | 1.33±1.29 | 0.480 |
| 正常受精卵率/% | 70±38 | 67±40 | 0.275 |
| 卵裂数 | 1.24±1.14 | 1.31±1.28 | 0.398 |
| 优质胚胎总数 | 0.71±0.91 | 0.74±0.94 | 0.030 |
| 有效胚胎总数 | 0.83±0.94 | 0.84±0.97 | 0.788 |
| 卵子利用率/% | 45±42 | 46±43 | 0.876 |
本研究回顾性分析了PPOS方案与CC微刺激方案在DOR患者接受IVF-ET治疗中的取卵周期结局。DOR患者的卵泡池中原始卵泡及对FSH敏感的卵泡已明显减少,生殖激素显示早卵泡期的FSH水平较高,振幅过大,LH持续时间延长,E2和P水平下降,与绝经过渡期描述的情况相似[16-17]。前期研究[14]显示,卵巢低反应患者易出现早发LH峰,而采用P后,此现象可以得到有效控制。本研究显示PPOS方案在用药初期,LH呈轻度上升趋势[D3: (4.33±1.90) U/L;D5~6: (5.12±2.76) U/L],这与p作用时间尚短,其负反馈作用尚未完全发挥相关。随着P使用时间的延长,其负反馈作用逐渐发挥,LH水平降低(P < 0.001)。而在促排卵后期,CC组患者LH水平则较基础水平明显升高。在对早发LH峰的统计中发现,PPOS组中有30例患者出现早发LH峰,而CC微刺激组中则有194例患者出现了早发LH峰(6.17% vs 39.92%, P < 0.001)。因此,PPOS方案中诱发排卵至取卵时间较CC组相对容易控制,且其更容易获得相对高的成熟卵率。这些结果提示DOR患者在促排卵过程中使用PPOS方案能有效抑制早发LH峰的出现。
临床实践发现,很多DOR患者在采用了CC微刺激方案后,由于过高的FSH水平和无卵泡发育,导致中途取消周期。而在PPOS方案中,P与位于下丘脑的P受体相结合,使GnRH的释放频率减慢,在发挥抑制早发LH峰发生的同时,也可在卵泡早期有效降低DOR患者过高的FSH水平。当FSH降至正常范围,E2慢慢上升,且卵巢有与之相匹配的基础卵泡时,采用外源性Gn来发挥促排卵作用。由于DOR患者对大剂量Gn反应欠佳,因此本研究选择小剂量hMG (75~150 U/d) 进行促排卵。本研究显示,DOR患者在接受PPOS治疗时,Gn的平均用量及时间明显大或长于CC组(P < 0.001)。这可能与CC本身具有促排卵作用,无需外源性Gn的添加相关。实验室结局显示两组患者在获卵数(率)、成熟卵数、正常受精卵数、卵裂数及有效胚胎数与CC组差异均无统计学意义。
综上所述,本研究结果显示PPOS方案可以有效抑制DOR患者促排卵过程中早发LH峰的发生,实验室结果显示该方案可获得与CC微刺激方案相似的卵子和可用胚胎。结果说明PPOS是一种适合DOR患者的促排卵方案,为DOR患者的临床用药提供了更多选择。今后将进一步回顾性分析两种方案所获得的胚胎移植后结局,并设计前瞻性多中心随机对照研究,进一步确定PPOS方案的临床有效性。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
BALASCH J. Ageing and infertility: an overview[J]. Gynecol Endocrinol, 2010, 26(12): 855-860.
[DOI]
|
| [2] |
MUTLU M F, ERDEM A. Evaluation of ovarian reserve in infertile patients[J]. J Turk Ger Gynecol Assoc, 2012, 13(3): 196-203.
[DOI]
|
| [3] |
LAND J A, YARMOLINSKAYA M I, DUMOULIN J C, et al. High-dose human menopausal gonadotropin stimulation in poor responders does not improve in vitro fertilization outcome[J]. Fertil Steril, 1996, 65(5): 961-965.
[DOI]
|
| [4] |
LEKAMGE D N, LANE M, GILCHRIST R B, et al. Increased gonadotrophin stimulation does not improve IVF outcomes in patients with predicted poor ovarian reserve[J]. J Assist Reprod Genet, 2008, 25(11-12): 515-521.
[DOI]
|
| [5] |
PAL L, JINDAL S, WITT B R, et al. Less is more: increased gonadotropin use for ovarian stimulation adversely influences clinical pregnancy and live birth after in vitro fertilization[J]. Fertil Steril, 2008, 89(6): 1694-1701.
[DOI]
|
| [6] |
JIRGE P R. Poor ovarian reserve[J]. J Hum Reprod Sci, 2016, 9(2): 63-69.
[DOI]
|
| [7] |
TERAMOTO S, KATO O. Minimal ovarian stimulation with clomiphene citrate: a large-scale retrospective study[J]. Reprod Biomed Online, 2007, 15(2): 134-148.
[DOI]
|
| [8] |
YU C M, DAI X L, WANG Y F, et al. Progestin-primed ovarian stimulation improves the outcomes of IVF/ICSI cycles in infertile women with diminished ovarian reserve[J]. J Chin Med Assoc, 2019, 82(11): 845-848.
[DOI]
|
| [9] |
FADDY M J, GOSDEN R G, GOUGEON A, et al. Accelerated disappearance of ovarian follicles in mid-life: implications for forecasting menopause[J]. Hum Reprod, 1992, 7(10): 1342-1346.
[DOI]
|
| [10] |
HSUEH A J, BILLIG H, TSAFRIRI A. Ovarian follicle atresia: a hormonally controlled apoptotic process[J]. Endocr Rev, 1994, 15(6): 707-724.
[URI]
|
| [11] |
Practice Committee of the American Society for Reproductive Medicine. Aging and infertility in women: a committee opinion[J]. Fertil Steril, 2002, 78(1): 215-219.
[DOI]
|
| [12] |
SAUER M V. The impact of age on reproductive potential: lessons learned from oocyte donation[J]. Maturitas, 1998, 30(2): 221-225.
[DOI]
|
| [13] |
HANSEN J P. Older maternal age and pregnancy outcome: a review of the literature[J]. Obstet Gynecol Surv, 1986, 41(11): 726-742.
[DOI]
|
| [14] |
CHEN Q, WANG Y, SUN L, et al. Controlled ovulation of the dominant follicle using progestin in minimal stimulation in poor responders[J]. Reprod Biol Endocrinol, 2017, 15(1): 71.
[DOI]
|
| [15] |
CUMMINS J M, BREEN T M, HARRISON K L, et al. A formula for scoring human embryo growth rates in in vitro fertilization: its value in predicting pregnancy and in comparison with visual estimates of embryo quality[J]. J In Vitro Fert Embryo Transf, 1986, 3(5): 284-295.
[DOI]
|
| [16] |
董骏鹏, 杨富. 前列腺素E2在排卵过程中作用及机制研究进展[J]. 中国临床医学, 2020, 27(3): 515-519. DONG J P, YANG F. Research progress on the role of prostaglandin E2 in ovulation and its mechanism[J]. Chinese Journal of Clinical Medicine, 2020, 27(3): 515-519. [URI] |
| [17] |
PAL L, ZHANG K, ZEITLIAN G, et al. Characterizing the reproductive hormone milieu in infertile women with diminished ovarian reserve[J]. Fertil Steril, 2010, 93(4): 1074-1079.
[DOI]
|
 2021, Vol. 28
2021, Vol. 28


