房颤是临床上最常见的快速性心律失常,其导致的脑卒中占所有脑卒中患者的20%左右,而脑卒中亦是房颤患者致死、致残的最主要原因。左心耳封堵术(left atrial appendage occlusion, LAAO)是近年来全球预防非瓣膜性房颤(non-valvular atrial fibrillation, NVAF)患者卒中的治疗新趋势,该技术能有效降低房颤患者的致死率、致残率,同时减少出血风险[1]。随着该技术的发展,临床上观察到左心耳解剖结构变异较大,主要表现为左心耳开口形态及内部形状的差异[2-3]。因此,在LAAO术前应进行充分的影像学评估,从而指导术中选择合适大小的封堵器。
目前,评估左心耳大小最常用的影像学方法有二维经食管超声心动图(two-dimensional transesophageal echocardiography, 2D-TEE)和数字减影血管造影(digital subtraction angiography, DSA)。TEE可以在术前准确评价患者心脏功能,评估心脏形态结构,在术中监测心脏功能,从而提高手术成功率[4]。2D-TEE在既往的LAAO文献[5]中主要用于测量左心耳开口最大直径,但测量结果估算的封堵器型号可能小于左心耳实际开口大小,导致器械更换率增加。研究[6]显示,3D-TEE能够充分显示左心耳开口、空间立体结构及分叶情况,从而获得更准确的左心耳开口直径数据,对选择合适大小的封堵器较2D-TEE更具优势;但该研究样本量仅30例,结果可能存在一定偏倚。本研究回顾性分析单中心接受LAAO治疗的NVAF患者,探讨3D-TEE、2D-TEE及DSA 3种方法测量的左心耳开口最大径与最终植入的左心耳封堵器大小的相关性,进一步探讨3D-TEE在LAAO术前评估中的应用价值。
1 资料与方法 1.1 研究对象回顾性选择2019年1月3日至2020年1月25日上海交通大学医学院附属新华医院接受择期LAAO的NVAF患者。纳入标准:(1)NVAF合并高卒中风险,CHA2DS2-VASc评分≥2分(表 1)或者HAS-BLED评分≥3分(表 2);(2)经诊断不宜长期服用抗凝类药物;(3)年龄≥18岁;(4)使用Watchman封堵器(美国波士顿科学公司)。排除标准:(1)左心耳内径>65 mm,经食管超声发现心内血栓或者左心耳重度自发显影者;(2)严重二尖瓣病变患者;(3)患有急性心肌梗死、下肢深静脉血栓、肺栓塞等需要使用抗凝类药物治疗的疾病。共筛选患者195例,排除15例,最终纳入180例。本研究获得上海交通大学医学院附属新华医院医学伦理委员会批准(XHEC-D-2024-004),并获得准许免除知情同意。
| Letter | Risk factors | Points |
| C | Congestive heart failure | 1 |
| H | Hypertension | 1 |
| A | Age≥75 years old | 2 |
| D | Diabetes | 1 |
| S | Stroke | 2 |
| V | Vascular disease | 1 |
| A | Age 65-74 years old | 1 |
| S | Sex(female) | 1 |
| Total points | 9 |
| Letter | Clinical characteristic | Points |
| H | Hpertension | 1 |
| A | Abnormal renal and liver function (1 point each) | 1 or 2 |
| S | Stroke | 1 |
| B | Bleeding | 1 |
| L | Labile INRs | 1 |
| E | Elderly (>65 years) | 1 |
| D | Drugs or alcohol | 1/2 |
| Total points | 9 | |
| HAS-BLED: hypertension, abnormal renal/liver function, stroke, bleeding history or predisposition, labile international normalized ratio, elderly (>65 years), drugs/alcohol concomitantly; INR: international normalized ratio. | ||
采用VividTM iq超声心动图仪(美国GE公司),6VT-D多平面经食管超声探头(3~6 MHz)进行心脏超声检查;Watchman左心耳封堵器,Watchman左心耳封堵器传送系统(美国波士顿科学公司)进行左心耳封堵手术;DSA数字减影机(德国西门子公司)进行术中造影。
1.3 超声检查及LAAO手术方法 1.3.1 术前食管超声检查患者禁食6 h、禁水4 h,检查前使用2%的盐酸利多卡因胶浆进行口咽部局部麻醉。检查时患者取左侧卧位,操作者将超声探头缓慢插入患者食管,深度距离门齿30~40 cm,最先获取左心耳0°切面,调整探头,继续观察45°、90°、135°切面,并充分显示左心耳及周围结构,观察左心房是否有自发显影及血栓形成。2D-TEE下充分显示左心耳后,适当调整探头,清晰显示左心耳冠状切面。手动启动3D-ZOOM prepare模式,显示出X-plane界面,同时显示左心耳相互垂直的两个切面,并调整取样框大小,使整个左心耳位于取样框内;取样线通过左心耳中轴线,点击3D-ZOOM成像,分别获得4个以上心动周期的超声动态图像。储存动态图像,并测量左心耳开口直径。食管超声的检查操作、数据测量和分析均由同一名有多年食管超声经验的心超医师完成。
1.3.2 LAAO手术患者取平卧位,接受全身麻醉和气管插管。操作者将食管超声探头经患者口咽部插入食管中段(距离门齿33~44 cm),观察左心耳及左心房有无血栓形成及自发显影程度,并从0°、45°、90°、135°观察左心耳。穿刺股静脉并置管,先行右心导管检查,测定肺动脉、右心室及右心房的压力。房间隔穿刺成功后送鞘管至左心房,精准测量左房压,并保持左心房平均压大于12 mmHg(1 mmHg=0.133 kPa)。静脉注射肝素并严密监测凝血活酶时间。将穿刺鞘管置入左上肺静脉,经鞘管送入260 cm加硬导丝,再沿导丝送入Watchman专用输送鞘管至左心房。将加硬导丝留置于左上肺静脉,撤出房间隔穿刺鞘,沿着导丝将封堵器输送鞘送至左上肺静脉,回撤导丝,将猪尾型导管输送鞘送入左上肺静脉,继而微调进入左心耳内,进行左心耳造影。采用DSA造影标准位测量左心耳开口直径、封堵器最终着陆区域的直径和左心耳的对应深度,包括右前斜位(RAO)30°+头位(CRA)20°和RAO 30°+足位(CAU)20°。术者参考影像学指标,凭经验选择合适大小的封堵器(一般封堵器直径比2D-TEE测量的最大开口直径大6 mm;比3D-TEE测量的最大开口直径大2~4 mm;比DSA测量的最大开口直径大4~6 mm)。顺导丝置入Watchman鞘管,退出导引钢丝及输送鞘内芯,定位后经输送鞘送入Watchman左心耳封堵器,缓慢回撤输送鞘展开封堵器,造影评估分流情况,推送数次显示封堵器固定良好。
1.3.3 LAAO成功封堵的标准为确保左心耳封堵器的稳定性、安全性和有效性,遵循PASS原则:(1)位置(Position),选择最佳锚定区,封堵器肩部置于左心耳口部;(2)锚定(Anchor),固定锚已嵌入左心耳壁,器械稳定,对封堵器进行有效的牵拉,以确定其稳定性;(3)尺寸(Size),器械压缩比=(原始尺寸-展开直径)/原始尺寸×100%,推荐压缩比为8%~20%;(4)密封(Seal),评估残余分流是否≤5 mm;在封堵器植入左心耳后,采用左心耳造影或者经食管超声来评估封堵器周围是否存在残余分流,并测量残余分流的宽度,若残余分流>5 mm,调整封堵器位置,调整后若分流仍未改善,更换大一型号的封堵器;封堵器与周边组织残余分流<3 mm定义为完全封堵。
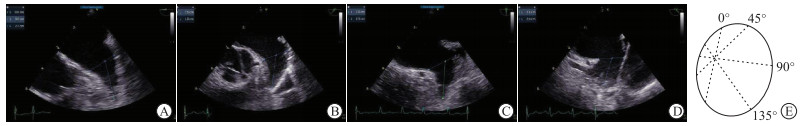
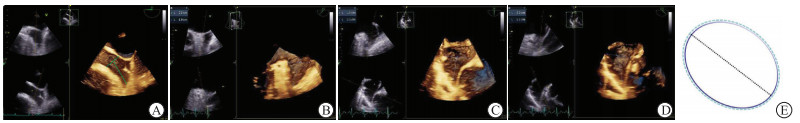
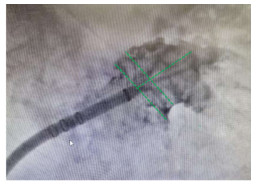
1.4 3D-TEE、2D-TEE、DSA测量指标及方法(1)2D-TEE测量左心耳开口最大直径、深度:左心耳开口直径为左回旋支(LCX)开口处至左上肺静脉脊下1.5~2 cm处的连线,深度为开口水平线的中点至左心耳尖部或者梳状肌上缘的距离,以上径线均在左心耳显示的最佳角度0°、45°、90°、135°进行测量(图 1)。(2)3D-TEE测量左心耳开口最大直径、深度:在左心耳冠状切面测量,左心耳开口直径为LCX开口处至左上肺静脉脊下1.5~2 cm处的连线,深度为开口水平线的中点至左心耳尖部或者梳状肌上缘的距离(图 2)。(3)DSA测量左心耳开口:测量左心耳开口最大直径、最小直径及深度(图 3)。
|
| 图 1 2D-TEE测量左心耳开口直径、深度和测量方法示意图 Fig 1 2D-TEE measurement of diameter and depth of left atrial appendage orifice and schematic diagram A-D: Imaging plane of left atrial appendage at different angles (0, 45, 90, 135 degrees, respectively); E: Schematic diagram of 2D-TEE measurement method (the green ellipse represents the left atrial appendage, the dashed line in the figure represents the diameter of the left atrial appendage orifice measured at different angles, and the dashed line at 135 degrees represents the maximum diameter of the left atrial appendage orifice). In image A-D, the short line represents the diameter of the left atrial appendage orifice, and the long line represents the depth of the left atrial appendage. The measured maximum diameter of left atrial appendage orifice is less than the actual maximum diameter by 2D-TEE. |
|
| 图 2 3D-TEE显示左心耳和左心耳开口直径测量方法示意图 Fig 2 3D-TEE shows left atrial appendage and schematic diagram of measuring diameter of left atrial appendage orifice A-D: The coronal section of the left atrial appendage at different angles (0, 45, 90, 135 degrees, respectively); the short line represents the diameter of the left atrial appendage orifice, and the long line represents the depth of the left atrial appendage; E: Schematic diagram of 3D-TEE measurement method (the black solid line ellipse represents the actual orifice of the left atrial appendage, while the black dashed line represents the maximum diameter of the left atrial appendage orifice). The actual maximum diameter of left atrial appendage orifice is measured, and circumference and area can also be measured by 3D-TEE. |
|
| 图 3 DSA测量左心耳开口直径和深度 Fig 3 DSA measurement of diameter and depth of left atrial appendage orifice |
采用SPSS 26.0软件进行统计学分析。符合正态分布的计量资料以x±s表示,计数资料以n(%)表示。采用Pearson相关分析评价不同影像学方法获得的左心耳开口最大直径与最终植入的左心耳封堵器大小的相关性,根据相关系数(r)判断相关性强弱,| r |<0.3为微弱相关,0.3≤| r |<0.5为低度相关,0.5≤| r |<0.8为中度相关,| r |≥0.8为高度相关[7]。检验水准(α)为0.05。
2 结果 2.1 研究对象一般资料结果(表 1)显示:180例NVAF患者中,男性112例、女性68例,年龄58~83岁,平均年龄(68.25±9.15)岁,体质量指数(body mass index, BMI)为(23.15±2.67)kg/m2,CHA2DS2-VASc评分(3.56±1.76)分,HAS-BLED评分(2.71±1.02)分。96例(53.3%)为持续性房颤;脑卒中病史9例(5%),糖尿病27例(15%),高血压146例(81.1%),冠心病34例(18.9%),房颤消融史22例(12.2%)。术前超声显示左心房最大前后内径(46.00±6.31)mm,双平面Simpson法测得的左心室射血分数(left ventricular ejection fraction, LVEF)为(61.90±6.25)%。
2.2 左心耳开口形态及分叶3种影像学方法观察左心耳开口形态中,鸡翅型82例(45.6%)、仙人掌型32例(17.7%)、风向袋型54例(30.0%)、菜花型12例(6.7%)。左心耳分叶中,1叶型36例(20.0%)、2叶型95例(52.8%),3叶型40例(22.2%),4叶型9例(5.0%)。
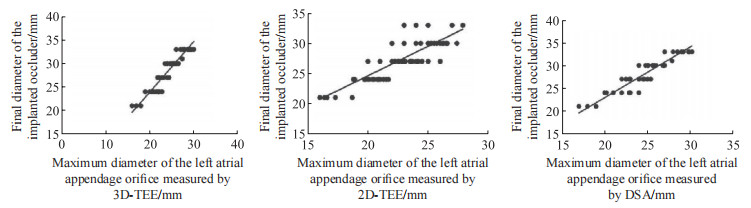
2.3 3D-TEE、2D-TEE、DSA测量的左心耳开口最大直径与实际植入封堵器大小的相关性分析180例患者均成功植入Watchman左心耳封堵器,最终植入的封堵器直径为(28.1±3.2)mm。术前3D-TEE测量的左心耳开口最大直径为(24.67±2.67)mm,显著高于2D-TEE测量的左心耳开口最大直径[(22.95±2.91)mm, P<0.001]和DSA测量的左心耳开口最大直径[(23.91±2.79)mm, P<0.001)]。Pearson相关分析(图 4)显示:3D-TEE测量的左心耳开口最大直径与最终植入封堵器大小高度相关(r=0.862, P<0.001);2D-TEE测量的左心耳开口最大直径与最终植入封堵器大小中度相关(r=0.614, P<0.001)。DSA测量的左心耳开口最大直径与最终植入封堵器大小中度相关(r=0.656, P<0.001)。
|
| 图 4 3D-TEE、2D-TEE、DSA测量左心耳开口最大直径与最终植入封堵器直径的相关性散点图 Fig 4 Scatter plot of the correlation between the maximum diameter of left atrial appendage orifice measured by 3D-TEE, 2D-TEE, DSA and the diameter of final implanted occluder |
| N=180 | |||||||||||||||||||||||||||||
| Characteristics | Results | ||||||||||||||||||||||||||||
| Age/year | 68.25±9.15 | ||||||||||||||||||||||||||||
| Male n(%) | 112(62.2) | ||||||||||||||||||||||||||||
| BMI/(kg·m-2) | 23.15±2.67 | ||||||||||||||||||||||||||||
| Classification of atrial fibrillation n(%) | |||||||||||||||||||||||||||||
| Permanent atrial fibrillation | 46(25.6) | ||||||||||||||||||||||||||||
| Paroxysmal atrial fibrillation | 38(21.1) | ||||||||||||||||||||||||||||
| Persistant atrial fibrillation | 96(53.3) | ||||||||||||||||||||||||||||
| CHA2DS2-VASc score | 3.56±1.76 | ||||||||||||||||||||||||||||
| HAS-BLED score | 2.71±1.02 | ||||||||||||||||||||||||||||
| Cardiac valve disease n(%) | 6(3.3) | ||||||||||||||||||||||||||||
| Stroke n(%) | 9(5.0) | ||||||||||||||||||||||||||||
| Hypertension n(%) | 146(81.1) | ||||||||||||||||||||||||||||
| Diabetes n(%) | 27(15.0) | ||||||||||||||||||||||||||||
| Coronary heart disease n(%) | 34(18.9) | ||||||||||||||||||||||||||||
| Hypertrophic cardiomyopathy n(%) | 7(3.9) | ||||||||||||||||||||||||||||
| Heart failure n(%) | 11(6.1) | ||||||||||||||||||||||||||||
| History of atrial fibrillation ablation n(%) | 22(12.2) | ||||||||||||||||||||||||||||
| Maximum anteriorposterior diameter of left atrium/mm | 46.00±6.31 | ||||||||||||||||||||||||||||
| LVEF/% | 61.90±6.25 | ||||||||||||||||||||||||||||
| BMI: body mass index; LVEF: left ventricular ejection fraction. | |||||||||||||||||||||||||||||
遵循PASS原则获得满意的封堵效果后,释放Watchman封堵器,封堵器压缩比(17.27±4.29)%。20例(11.1%)患者存在1~3 mm的残余分流,125例(69.4%)存在允许的露肩,22例(12.2%)术后检测出微量心包积液。
3 讨论LAAO手术通过微创的方式,将封堵器植入左心耳,从而预防房颤患者血栓形成。选择合适的封堵器是确保LAAO手术安全、有效的关键,而准确测量左心耳开口直径对封堵器选择和手术顺利进行至关重要[8]。本研究回顾性分析180例LAAO患者的数据,比较不同影像学方法测量左心耳开口直径与最终植入封堵器大小的相关性,结果显示,3D-TEE测量的左心耳开口最大直径与最终植入的左心耳封堵器大小的相关性最强。
临床上评估左心耳开口内径的影像学方法有TEE、DSA、计算机断层血管造影(computed tomography angiography, CTA)和心腔内超声(intracardiac echocardiography, ICE),其中TEE和DSA较为常用[9]。TEE在临床应用广泛,技术较为成熟,能在术前评估左心耳内血栓和自发显影程度,且在封堵器释放前可以检测封堵器的压缩比和稳定性。目前,临床上较多地应用2D-TEE来测量左心耳开口的最大直径,并在此基础上选择封堵器型号。3D-TEE通过三维全容积成像,可以充分显示左心耳开口全貌,包括左心耳解剖形态、分叶数、内部及周围结构,并实现任意角度测量;相较于二维平面模式下固定角度的测量,3D-TEE的可选择性更广、准确性更高,也能更加精确测量左心耳开口直径[10]。
本研究结果显示,3D-TEE测量的左心耳开口最大直径显著大于2D-TEE测量的结果,术前2D-TEE对左心耳开口直径的测量值偏小,可能的原因有:(1)左心房大小易受容量负荷影响,每增加1 000 mL的液体量,左心房的直径和深度增加约2 mm[11]。食管超声检查前一般至少禁食6 h、禁水4 h,患者液体补充不足、血容量减少,导致左心房压力下降,左心房及左心耳各径线数值减小;而术中为保证左心耳的充盈状态,需常规补液以维持左房压力>12 mmHg[12],左心耳开口直径增加。(2)左心耳的形态复杂及开口形状多变,2D-TEE难以准确扫查其开口最大径所在平面。不同的左心耳平面测量出的开口最大径不同,其测量平面的差异导致了测量结果的差异。左心耳开口测量平面有二尖瓣环、左冠状动脉回旋支、左上肺静脉外侧脊水平,其中左肺静脉脊的形态多不规则,与二尖瓣环的连贯性较差;二维成像技术每个角度只对应单一平面的测量,测量准确性欠佳,致使2D-TEE常低估左心耳开口大小。(3)术前2D-TEE的测量平面未能和术中封堵器的着陆平面保持一致,导致测量数据存在误差。Streb等[13]研究显示,与2D-TEE相比,应用3D-TEE测量左心耳开口最大直径的测量重复性更好、差异度更小,并且与最终植入的封堵器有更好的相关性。3D-TEE可以实现从不同平面、不同角度来观察左心耳的开口,在2D-TEE的基础上通过3D-ZOOM模式、X-Plane平面来充分显示左心耳的三维立体结构,通过裁剪取样框选取感兴趣区域进行重点分析,测量各项数值的大小,筛选出左心耳的最佳测量平面,即左心耳的锚定区域平面;因此,3D-TEE在左心耳开口的测量上相对更准确。
此外,本研究发现3D-TEE测量的左心耳开口最大直径大于DSA测量的数值,原因可能为X线下投影角度的关系,DSA获取的测量平面并非左心耳开口的冠状切面,所选取切面并不一定是左心耳开口最大径线切面,从而造成测量值偏小。因此,2D-TEE测量左心耳开口内径会存在着一定的偏差,而3D-TEE能够更加全面地显示左心耳开口的立体解剖形态,并对左心耳进行精确的分析测量。
Watchman封堵器的型号选择和成功植入必须以术前、术中对左心耳开口直径进行精确测量为基础,型号一般大于影像学方法测得的左心耳开口最大直径的10%~20%。左心耳的解剖结构个体差异较大[14],其内部形状、开口大小、分叶数、尖部所在方位都不尽相同。Wang等[15]从拟行导管消融的房颤患者中总结出了左心耳常见的4种类型,分别为鸡翅型、风向袋型、仙人掌型和菜花型。其中,鸡翅形最常见,菜花型更容易形成心耳血栓导致脑卒中。封堵难易度方面,菜花型的左心耳短而小、开口大、分叶多,深度小于开口最大径,较难封堵;鸡翅型左心耳只有一个主叶,主叶近中部出现弯曲或者反折,封堵时也具有一定难度。本研究中的180例LAAO患者中,鸡翅型82例(46%)、仙人掌型32例(17.7%)、风向袋型54例(30%)、菜花型13例(7.2%)。若存在左心耳内梳状肌过于丰富,个别梳状肌体积大,或者梳状肌突入开口处等情况,会增加封堵器植入的难度,并进一步影响封堵器的稳定性和实际封堵的效果。本研究有5例患者术前3D-TEE显示:距离左心耳开口较近处有粗大的梳状肌横行于左心耳腔,且将左心耳分割成2个腔,导致术中封堵器植入难度增加,封堵器边缘的倒刺经多次旋转后才稳定地挂靠在左心耳壁。因此,术前应用3D-TEE对左心耳的形态和梳状肌进行准确评估显得尤为重要。
本研究存在一定局限性:(1)仅采用3D-TEE、2D-TEE、DSA比较了左心耳开口最大直径这一数值,未纳入左心耳开口最小直径、深度等数值的比较;(2)纳入的患者均接受塞式封堵器,缺乏盘式封堵器的相关数据;(3)为回顾性研究,缺乏长期随访数据,未来可进行前瞻性的随机对照研究,验证本研究结果。
综上所述,3D-TEE通过三维容积成像测量的左心耳开口最大直径显著高于2D-TEE和DSA测量的最大直径,且与成功植入的封堵器大小的相关性最强。3D-TEE可以较好地应用于LAAO前左心耳开口大小的评估。
伦理声明 本研究获得上海交通大学医学院附属新华医院医学伦理委员会批准(XHEC-D-2024-004)。
利益冲突 所有作者声明不存在利益冲突。
作者贡献 杨晓敏:收集整理数据、统计分析和撰写论文;刘博:研究选题和论文审查修改。
| [1] |
HOLMES D R, KORSHOLM K, RODÉS-CABAU J, et al. Left atrial appendage occlusion[J]. EuroIntervention, 2023, 18(13): e1038-e1065.
[DOI]
|
| [2] |
LUPERCIO F, RUIZ J C, BRICENO D F, et al. Left atrial appendage morphology assessment for risk stratification of embolic stroke in patients with atrial fibrillation: a meta-analysis[J]. Heart Rhythm, 2016, 13(7): 1402-1409.
[DOI]
|
| [3] |
TZIKAS A, HOLMES D R, GAFOOR S, et al. Percutaneous left atrial appendage occlusion: the Munich consensus document on definitions, endpoints, and data collection requirements for clinical studies[J]. Europace, 2017, 19(1): 4-15.
|
| [4] |
白炜, 孟欣, 康楠, 等. 术中经食管超声心动图对心脏瓣膜置换术后即刻评估的价值研究[J]. 中国医学装备, 2021, 18(3): 81-84. BAI W, MENG X, KANG N, et al. Study on the value of intraoperative transesophageal echocardiography on the postoperatively immediate assessment of heart valve replacement[J]. Chin Med Equip, 2021, 18(3): 81-84. [CNKI] |
| [5] |
潘翠珍, 周达新, 张晓春, 等. 经食管超声心动图在心房颤动行左心耳封堵术中的应用[J]. 中国介入心脏病学杂志, 2019, 27(4): 181-186. PAN C Z, ZHOU D X, ZHANG X C, et al. Application of transesophageal echocardiography in left atrial appendage occlusion for atrial fibrillation[J]. Chin J Intervent Cardiol, 2019, 27(4): 181-186. [CNKI] |
| [6] |
汤跃跃, 张容亮, 杨寒凝, 等. 经食管实时三维及二维超声心动图在左心耳封堵围术期的应用[J]. 中国医学影像学杂志, 2021, 29(4): 339-342. TANG Y Y, ZHANG R L, YANG H N, et al. Application of real-time three-dimensional and two-dimensional transesophageal echocardiography in peri-operative of transcatheter left atrial appendage occlusion[J]. Chin J Med Imaging, 2021, 29(4): 339-342. [CNKI] |
| [7] |
罗允内. 房性心律失常代偿间歇及联律间期与窦房结功能相关性研究[D]. 广东: 广东中医药大学, 2015. LUO Y N. A study on the correlation between compensatory intervals and synrhythmic intervals of atrial arrhythmias and sinus node function[D]. Guangdong: Guangdong University of Traditional Chinese Medicine, 2015. |
| [8] |
WUNDERLICH N C, BEIGEL R, SWAANS M J, et al. Percutaneous interventions for left atrial appendage exclusion: options, assessment, and imaging using 2D and 3D echocardiography[J]. JACC Cardiovasc Imaging, 2015, 8(4): 472-488.
[DOI]
|
| [9] |
肖玲娜, 曾安宁, 罗勇, 等. CT双期增强扫描用于心房颤动患者左心耳血栓诊断的临床观察[J]. 中华全科医学, 2022, 20(10): 1733-1736. XIAO L N, ZENG A N, LUO Y, et al. Study on the clinical effect of dual phase enhanced CT scanning in the diagnosis of left atrial appendage thrombosis in patients with atrial fibrillation[J]. Chin J Gen Pract, 2022, 20(10): 1733-1736. [CNKI] |
| [10] |
吴阳. 经食道超声心动图三维成像与CT容积再现技术在左心耳封堵术中应用价值的对比研究[D]. 大连: 大连医科大学, 2021. WU Y. Comparative study on the application value of transesophageal echocardiography three-dimensional imaging and CT volume reconstruction technology in left atrial appendage occlusion[D]. Dalian: Dalian Medical University, 2021. |
| [11] |
AL-KASSOU B, TZIKAS A, STOCK F, et al. A comparison of two-dimensional and real-time 3D transoesophageal echocardiography and angiography for assessing the left atrial appendage anatomy for sizing a left atrial appendage occlusion system: impact of volume loading[J]. EuroIntervention, 2017, 12(17): 2083-2091.
[DOI]
|
| [12] |
GLIKSON M, WOLFF R, HINDRICKS G, et al. EHRA/EAPCI expert consensus statement on catheter-based left atrial appendage occlusion—an update[J]. EuroIntervention, 2020, 15(13): 1133-1180.
[DOI]
|
| [13] |
STREB W, MITRĘGA K, PODOLECKI T, et al. Two-dimensional versus three-dimensional transesophageal echocardiography in percutaneous left atrial appendage occlusion[J]. Cardiol J, 2020, 26(6): 687-695.
[DOI]
|
| [14] |
KORSHOLM K, BERTI S, IRIART X, et al. Expert recommendations on cardiac computed tomography for planning transcatheter left atrial appendage occlusion[J]. JACC Cardiovasc Interv, 2020, 13(3): 277-292.
[DOI]
|
| [15] |
WANG Y, DI BIASE L, HORTON R P, et al. Left atrial appendage studied by computed tomography to help planning for appendage closure device placement[J]. J Cardiovasc Electrophysiol, 2010, 21(9): 973-982.
[DOI]
|
 2024, Vol. 31
2024, Vol. 31


