横纹肌肉瘤(rhabdomyosarcoma, RMS)是一类起源于中胚层的罕见恶性肿瘤,一般见于儿童,成人罕见[1]。多形性横纹肌肉瘤(pleomorphic rhabdomyosarcoma, PRMS)是RMS的一种少见亚型,其恶性程度较高、预后较差,患者长期生存率低[2]。目前,国内外关于PRMS的报道有限且多为个案分析,临床上对该病缺乏全面的认识,且易与其他类型RMS、未分化多形性肉瘤(undifferentiated pleomorphic sarcoma, UPS)、多形性平滑肌肉瘤(pleomorphic leiomyosarcoma)及其他伴有横纹肌样分化的上皮和间叶源性恶性肿瘤相混淆,导致诊断困难[1]。本研究回顾性分析2008年6月至2023年3月苏州大学附属第一医院收治的6例PRMS,探讨PRMS的临床病理特征、影像学表现、免疫表型及鉴别诊断要点等,旨在提高临床医师及病理医师对该病的认识水平,从而实现准确诊断、尽早治疗,延长患者生存期的目的。
1 资料与方法 1.1 研究对象回顾性收集2008年6月至2023年3月经苏州大学附属第一医院诊断的6例PRMS患者的临床及病理资料,并进行随访。
1.2 资料收集及随访所有患者的临床资料通过调阅电子病历档案获得,包括年龄、性别、症状、发病部位和影像学表现,所有病例的病理切片均由2名高年资病理科医师复核诊断。采用电话随访,随访内容包括患者生存状态,有无局部复发或全身转移,随访截止日期为2023年3月31日。
1.3 方法标本均用10%中性甲醛固定,常规石蜡包埋,以4 μm厚度制片,进行H-E染色。采用EnVision两步法进行免疫组化染色,一抗包括购自Dako公司的结蛋白(desmin)、平滑肌肌动蛋白(SMA)、细胞角蛋白(CK)、上皮膜抗原(EMA)、S-100蛋白(S-100)、白细胞共同抗原(LCA)、CD20、CD3、间变性淋巴瘤激酶(ALK),购自北京中杉金桥生物技术有限公司的肌生成素(myogenin)、肌源性调节蛋白(MyoD1)、CD99、CD4,购自基因科技(上海)股份有限公司的Ki-67和黑色素标志物(HMB-45、Melan-A)。具体操作步骤严格按试剂盒说明书进行,并设阴性和阳性对照。免疫组化阳性定位:MyoD1、myogenin和Ki-67标记的阳性信号定位于细胞核,S-100定位于细胞核及细胞质,EMA、CD99、LCA、CD20定位于细胞膜,CD3、CD4定位于细胞膜及细胞质,其他标志物均定位于细胞质。
2 结果 2.1 临床特征结果(表 1)显示:6例PRMS患者中,男性5例、女性1例,男女比例5∶1;年龄29~77岁,平均年龄54.17岁,中位年龄55岁。2例患者缺少症状描述和影像学资料;其余4例患者中,病例3因“自觉颌下肿物进行性增大伴疼痛”入院;病例4因“无明显诱因出现右肩背部肿块,受外力击打后进行性增大并伴压痛”入院,病例5因“无明显诱因出现右臀部肿块进行性增大、质硬、不可活动,压之无疼痛”入院;病例6因“无明显诱因出现涕中带血(无面部麻木、复视、耳闷、耳鸣),症状持续伴喉部异物感”入院。所有患者入院后均完善CT或MRI检查,评估肿块大小及侵袭范围,初步判断肿块性质。6例PRMS患者发病部位依次为右上臂、右肾盂、左鼻窦/颈部/下颌、右肩背、右臀大肌、鼻咽部。
| Case number | Gender | Age/year | Symptoms | Tumor location | Imaging | Follow-up |
| 1 | Male | 77 | Lack of data | Right upper arm | Lack of data | Loss to follow-up |
| 2 | Female | 47 | Lack of data | Right renal pelvis | Lack of data | Loss to follow-up |
| 3 | Male | 29 | Progressive enlargement of submaxillary mass | Left sinus/neck/ lower mandible | CT: space-occupying lesion on the left neck, enlargement of the left submandibular lymph node | 33 months (lymphatic metastasis) |
| 4 | Male | 44 | Increased mass in the right shoulder and back | Right shoulder and back | MRI: space occupying with focal bleeding | 6 months (recurrence) |
| 5 | Male | 63 | Increased mass in the right hip | Right gluteus maximus | MRI: subcutaneous space occupying lesion | 18 months (recurrence) |
| 6 | Male | 65 | Blood in the nose and abnormal sensation in the throat | Nasopharynx | MRI plain scan + enhancement: lumps with long T1 and slightly longer T2 signal, showing lobulation, unclear boundary with soft palate, and obvious enhancement after enhanced scan | 64 months (recurrence) |
| CT: computed tomography; MRI: magnetic resonance imaging; PRMS: pleomorphic rhabdomyosarcoma. | ||||||
6例PRMS均手术切除,肿块最大径0.5~12 cm,肿块切面为灰白或灰白伴灰黄,2例质嫩或细腻,2例肉眼可见坏死,1例境界清。
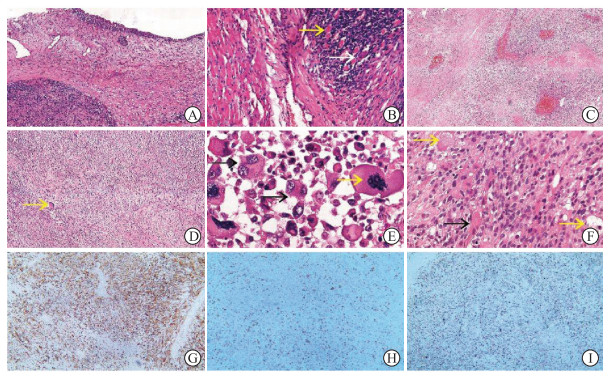
2.2.2 组织形态肿瘤细胞丰富(图 1A),呈浸润性生长(图 1B);凝固性坏死常见(3/6, 50%;图 1C),其中1例坏死主要发生于远离血管区(图 1C)。2例以异型的梭形细胞为主,呈束状、席纹状排列,其间可见散在多形性大细胞(图 1D)。可见显著异型的大细胞性横纹肌母细胞,胞质丰富深嗜伊红,无横纹(图 1B),以及多核、巨核瘤细胞,染色质粗糙,核分裂象易见(图 1E)。4例呈典型的多形性肉瘤形态,瘤细胞形状不规则,可为圆形、多边形及梭形,部分梭形细胞胞质内可见横纹(图 1F)。
|
| 图 1 PRMS的组织学形态及免疫表型 Fig 1 Histological morphology and immunophenotyping of PRMS A: PRMS occurs submucous in the renal pelvis and is rich of tumor cells (case 2); B: Invasive growth, residual skeletal muscle (yellow arrow) and scattered macrocellular pleomorphic rhabdomyoblasts (PRMB, white arrow) can be seen (case 4); C: Coagulation necrosis of the PRMS occuring in area far away from blood vessels (case 5); D: PRMS is dominated by spindle cells, with large pleomorphic cells (yellow arrow) scattered among them (case 4); E: The tumor cells are polymorphic, showing megacellular PRMB with mitosis (yellow arrow), and the polymorphic multinucleoma giant cells (black arrow) with large nuclei (case 3); F: Large vacuoles can be seen in the cytoplasm of PRMB, in the shape of "spider web" (yellow arrow), and transverse lines can be seen in some spindle cells (black arrow, case 5); G: Diffuse expression of desmin (case 5); H: Focal expression of MyoD1 (case 1); I: Ki-67 is 70% (case 1). A-F: H-E staining; G-I: Immunohistochemical staining. PRMS: pleomorphic rhabdomyosarcoma; PRMB: pleomorphic rhabdomyoblasts. Original magnification: ×50 (A, D); ×100 (B, G, H); ×25 (C); ×400 (E); ×200 (F); ×40 (I). |
6例(100%)弥漫表达desmin(图 1G),5例(83.3%)灶性表达myogenin,4例(66.7%)灶性表达MyoD1(图 1H),1例(16.7%)灶性表达SMA,Ki-67增殖指数30%~70%(平均50%;图 1I)。另一些上皮(CK、EMA)、神经(S-100)、黑色素(S-100、HMB45、Melan-A)及小圆细胞(CD99、LCA、CD20、CD3、CD4)等的标志物均为阴性。
2.3 治疗及随访6例PRMS患者均接受手术治疗;4例患者获得完整随访资料,2例(病例1、病例2)失访。病例3接受肿块切除+颈淋巴结清扫术,术后进行放化疗(采用异环磷酰胺、表柔比星、达卡巴多疗程联合化疗方案),2年后复发伴淋巴结转移;病例4接受手术切除联合术后放疗,术后3个月复发,再次手术后复发(术后2个月);病例5接受手术切除联合术后放化疗(采用紫杉醇、表柔比星等多疗程联合化疗方案),复发;病例6接受手术联合放疗,反复复发,共手术切除10余次。4例患者放疗剂量45~60 Gy,生存时间6~64个月,最终均死亡。
3 讨论 3.1 RMS分型RMS是一类罕见的软组织恶性肿瘤,随着研究增多及分子遗传学的发展,其分型不断完善。2020版WHO RMS分型[2]延续了2013版的4个亚型:胚胎型(ERMS)、腺泡型(ARMS)、梭形细胞/硬化型(SRMS)和多形性(PRMS)。近年来,一些新的亚型被陆续报道。Watson等[3]报道了一种新的RMS亚型,其倾向于骨内发生,主要见于颅面骨,遗传特征为EWSR1/FUS: : TFCP2基因融合,具有梭形及上皮样的形态,在所有年龄段均可发生,阳性表达上皮标志物(CK或EMA),过表达ALK,被暂时归类在SRMS亚型中;Agaram等[4]则报道了另一组具有MEIS1:: NCOA2融合基因的骨原发RMS。
3.2 PRMS病理学特征PRMS作为RMS的一种罕见亚型,最早由Stout[5]报道。PRMS诊断标准:肿瘤细胞呈多边形、圆形和梭形,可见骨骼肌分化,且没有胚胎或腺泡成分[6]。多数可见数量不等的多形性横纹肌母细胞(PRMB),其为显著异型的大细胞,胞质丰富深嗜伊红,无横纹,可见大的多形性核;因此,发现PRMB对PRMS具有诊断意义[7]。根据瘤细胞组成,Furlong等[8]将PRMS分为3种类型:Ⅰ型或“经典PRMS”,由片状PRMB组成,瘤巨细胞及多核瘤细胞常见;Ⅱ型或“圆形细胞PRMS”,主要由成簇的大圆形或大多边形PRMB组成,背景中见轻度多形的中等大小的圆形PRMB;Ⅲ型或“梭形细胞PRMS”,高度纺锤状异型梭形细胞呈席纹状或条束状排列,可见散在诊断性大细胞性PRMB,免疫组化弥漫表达desmin,而myogenin和MyoD1表达局限。本研究6例PRMS中,4例呈典型的多形性肉瘤形态;2例以异型的梭形细胞为主,其间可见散在多形性大细胞,两者之间存在移行过渡;6例(100%)弥漫表达desmin,5例(83.3%)灶性表达myogenin,4例(66.7%)灶性表达MyoD1。
3.3 PRMS临床特征PRMS发病率低,多发生于下肢深部软组织内,肿瘤体积大(最大径5~12 cm),预后差,局部生长和转移的患者中位生存期分别为12.8个月和7.1个月[9]。喻林等[7]统计了2005年至2012年复旦大学附属肿瘤医院收治的所有RMS患者,发现PRMS占8.7%。苏州大学附属第一医院2008年至2023年收治的RMS患者共66例,其中PRMS为6例,占比9.09%。Deb等[10]通过查询SEER数据库,发现在符合诊断标准的242例PRMS患者中,大多数年龄在40岁以上,且男性多于女性(男女比例约3∶2);肿瘤部位对疾病预后无特异性影响。本研究中,患者以男性为主,除病例3为29岁年轻男性,其余病例均在40岁以上,与以往报道一致。PRMS多见于四肢,其次为躯干,少数可发生于实质脏器和头颈部[9],其症状因发生部位不同而异,主要表现为肿块快速增大,可伴疼痛、不适、出血及肢体麻木,少数无特异症状,多为偶然发现[7]。本研究的6例PRMS患者中,3例发生于四肢及躯干,2例发生于鼻咽鼻窦部,1例发生于实质脏器。
3.4 PRMS起源及发病机制PRMS的起源及发病机制复杂,目前仍不明确。近年来的分子遗传学数据为RMS的病因和发病机制提供了大量信息。与RMS的其他亚型不同,PRMS缺乏特异性染色体易位或基因突变[3]:PRMS缺乏MyoD1基因的体细胞突变或PAX和FOXO1的重排,而这些可能分别在SRMS或ARMS中检测到;PRMS不会出现超倍体,而ERMS可能出现;排除其他类型RMS后,分子遗传学的阴性结果可以支持PRMS诊断。Goldstein等[11]使用光谱核型比较基因组杂交和表达分析,研究了10例原发性RMS肿瘤(其中1例为PRMS),发现PRMS肿瘤中LAMC2和PAK1(参与基底膜和细胞骨架的调节)的拷贝数增加以及GLI(编码转录因子)缺失,认为PRMS肿瘤发生涉及细胞黏附、细胞骨架信号转导、转录等诸多基因。Machado等[12]用Ptch1+/-/ETV7TG+/-小鼠来构建PRMS模型,结果表明,神经氨酸酰化酶1的功能降低,导致溶酶体外排作用增加(肿瘤及基质细胞溶酶体相关膜蛋白1重新分布到细胞膜上),其具体致瘤机制有待进一步研究。比较基因组原位杂交(CGH)检测到8个高度扩增的区域1p36.1-p36.2、1p31-p32、1q21-q31、8q12-q21、8q24-qter、11q12-q13、12q13-q14和18q12-q22,提示至少有8个扩增的致癌基因可能参与PRMS发病[13]。另外,在PRMS患者的组织样本中,MyoD1和myogenin的mRNA高表达[14]。上述研究对PRMS的发病机制具有提示作用,目前尚未应用于临床诊断。研究[15-16]显示,大多数肉瘤发生于间充质干细胞(MSCs)及其衍生细胞系的异常分化过程,其具体机制还有待进一步探究。
3.5 PRMS鉴别诊断PRMS需与其他亚型RMS相鉴别[2]:(1)ERMS,RMS最常见的亚型,好发于15岁以下,男女比例1.4∶1,多见于头颈部及泌尿、生殖系统,预后较好。组织学上呈原始的小蓝圆细胞至有一定分化、具有嗜酸性胞质的卵圆形细胞、短梭形细胞,胞质少,细胞紧密排列成片状,或可见大量疏松的黏液样背景。(2)ARMS,好发于10~20岁青少年,男女比例相近,多见于四肢,预后较差。组织学上为单形性的原始肿瘤细胞,核为圆形,纤维血管间隔将肿瘤细胞分割,呈腺泡样。免疫组化desmin强阳性,myogenin和MyoD1弥漫强阳性。(3)SRMS,好发于婴幼儿、儿童及成年人,多见于头颈部及四肢,组织学上为较为一致呈长束状排列的梭形细胞,可见玻变的硬化性区域,而PRMS多形性显著,缺乏硬化区域。(4)PRMS与未分化多形性肉瘤(UPS)形态学相似,易误诊,但UPS中大嗜酸性细胞胞质呈细空泡状,且可见组织细胞、破骨样巨细胞和炎细胞,而PRMS大嗜酸性PRMB胞质内可见粗大空泡,呈“蜘蛛网”状;免疫组化染色UPS表现为desmin局灶阳性,而myogenin和MyoDl阴性,与PRMS不同[7]。(5)多形性平滑肌肉瘤镜下也可见多形性细胞,可见典型平滑肌肉瘤细胞特征,且其免疫组化示MSA、SMA阳性,而myogenin和MyoDl阴性。(6)伴有横纹肌样分化的上皮及间叶源性恶性肿瘤,如去分化脂肪肉瘤、骨肉瘤、软骨肉瘤、Sertoli-Leydig细胞瘤、恶性外周神经鞘膜瘤等,此类肿瘤可见典型的非RMS区域,而非单纯的PRMS,配合相应免疫组化,鉴别困难不大。鉴于PRMS罕见且鉴别诊断复杂,充分取材、准确诊断尤为必要,必要时可进行分子检测。
3.6 PRMS治疗及预后PRMS恶性程度高,患者生存率低,目前临床尚无标准的系统化治疗方法,多采用手术切除联合化学治疗,放射治疗敏感性欠佳[17]。Liu等[18]报道了1例PD-L1阳性的PRMS患者在接受免疫治疗后获得45个月的无复发生存期,免疫治疗或将成为PRMS患者的有效治疗途径,且PD-L1表达及T细胞浸润可能成为PRMS患者免疫治疗有效性评估的潜在生物标志物。
综上所述,PRMS发病率极低,预后较差。镜下肿瘤细胞呈多边形、圆形和梭形,无胚胎或腺泡成分,发现PRMB对PRMS具有诊断意义,免疫组化有助于鉴别诊断,必要时可辅助分子检测,提高确诊率。
伦理声明 无。
利益冲突 所有作者声明不存在利益冲突。
作者贡献 马妍:设计研究、采集及分析数据、撰写文章;郭凌川:复核病理切片、解释数据、审阅文章、指导;黄山:复核病理切片、解释数据、审阅文章;杨倩倩:设计研究、分析及解释数据、统计分析、获取研究经费、指导研究。
| [1] |
AGARAM N P. Evolving classification of rhabdomyosarcoma[J]. Histopathology, 2022, 80(1): 98-108.
[DOI]
|
| [2] |
World Health Organization (WHO). WHO classification of tumours: soft tissue and bone tumours. 5th ed[M]. Lyon, France: IARC press, 2020.
|
| [3] |
WATSON S, PERRIN V, GUILLEMOT D, et al. Transcriptomic definition of molecular subgroups of small round cell sarcomas[J]. J Pathol, 2018, 245(1): 29-40.
[DOI]
|
| [4] |
AGARAM N P, ZHANG L, SUNG Y S, et al. Expanding the spectrum of intraosseous rhabdomyosarcoma: correlation between 2 distinct gene fusions and phenotype[J]. Am J Surg Pathol, 2019, 43(5): 695-702.
[DOI]
|
| [5] |
STOUT A P. Rhabdomyosarcoma of the skeletal muscles[J]. Ann Surg, 1946, 123(3): 447-472.
[DOI]
|
| [6] |
FLETCHER C D, UNNI K K, MERTENS F. World Health Organization classification of tumours: patholoy and genetics of tumours of soft tissue and bone[M]. Lyon, France: IARC Press, 2002: 153-154.
|
| [7] |
喻林, 王坚. 多形性横纹肌肉瘤的临床病理学观察[J]. 中华病理学杂志, 2013, 42(3): 147-152. YU L, WANG J. Clinicopathologic features of pleomorphic rhabdomyosarcoma[J]. Chin J Pathol, 2013, 42(3): 147-152. [DOI] |
| [8] |
FURLONG M A, MENTZEL T, FANBURG-SMITH J C. Pleomorphic rhabdomyosarcoma in adults: a clinicopathologic study of 38 cases with emphasis on morphologic variants and recent skeletal muscle-specific markers[J]. Mod Pathol, 2001, 14(6): 595-603.
[DOI]
|
| [9] |
CARVALHO S D, PISSALOUX D, CROMBÉ A, et al. Pleomorphic sarcomas: the state of the art[J]. Surg Pathol Clin, 2019, 12(1): 63-105.
[DOI]
|
| [10] |
DEB P Q, CHOKSHI R J, LI S, et al. Pleomorphic rhabdomyosarcoma: a systematic review with outcome analysis and report of a rare abdominal wall lesion[J]. Int J Surg Pathol, 2023, 31(5): 548-556.
[DOI]
|
| [11] |
GOLDSTEIN M, MELLER I, ISSAKOV J, et al. Novel genes implicated in embryonal, alveolar, and pleomorphic rhabdomyosarcoma: a cytogenetic and molecular analysis of primary tumors[J]. Neoplasia, 2006, 8(5): 332-343.
[DOI]
|
| [12] |
MACHADO E R, VAN DE VLEKKERT D, SHEPPARD H S, et al. Haploinsufficiency of the lysosomal sialidase NEU1 results in a model of pleomorphic rhabdomyosarcoma in mice[J]. Commun Biol, 2022, 5(1): 992.
[DOI]
|
| [13] |
TAKAOKA E, SONOBE H, AKIMARU K, et al. Multiple sites of highly amplified DNA sequences detected by molecular cytogenetic analysis in HS-RMS-2, a new pleomorphic rhabdomyosarcoma cell line[J]. Am J Cancer Res, 2012, 2(2): 141-152.
|
| [14] |
LI G D, OGOSE A, KAWASHIMA H, et al. Cytogenetic and real-time quantitative reverse-transcriptase polymerase chain reaction analyses in pleomorphic rhabdomyosarcoma[J]. Cancer Genet Cytogenet, 2009, 192(1): 1-9.
[DOI]
|
| [15] |
EID J E, GARCIA C B. Reprogramming of mesenchymal stem cells by oncogenes[J]. Semin Cancer Biol, 2015, 32: 18-31.
[DOI]
|
| [16] |
LYE K L, NORDIN N, VIDYADARAN S, et al. Mesenchymal stem cells: from stem cells to sarcomas[J]. Cell Biol Int, 2016, 40(6): 610-618.
[DOI]
|
| [17] |
NOUJAIM J, THWAY K, JONES R L, et al. Adult pleomorphic rhabdomyosarcoma: a multicentre retrospective study[J]. Anticancer Res, 2015, 35(11): 6213-6217.
|
| [18] |
LIU J Y, LIU P J, GONG F Y, et al. Case report: a PD-L1-positive patient with pleomorphic rhabdomyosarcoma achieving an impressive response to immunotherapy[J]. Front Immunol, 2022, 13: 815598.
[DOI]
|
 2024, Vol. 31
2024, Vol. 31


