2. 复旦大学附属中山医院肝外科, 上海 200032
2. Department of Liver Surgery, Zhongshan Hospital, Fudan University, Shanghai 200032, China
肝细胞肝癌(HCC)是起源于肝实质细胞的肝癌,发病率占原发性肝癌的85%~90%,是终末期肝病患者的主要死亡原因之一。乙型肝炎病毒感染、丙型肝炎病毒感染、脂肪肝、糖尿病、过量摄入酒精或黄曲霉含量过高的食物等都是导致HCC的危险因素[1]。在全球范围内,HCC的发病率在所有肿瘤中排第6位,致死率排第3位[2];在我国,HCC的发病率在所有恶性肿瘤中排第4位,致死率排第3位,且HCC患者占全球50%以上[3]。
目前HCC的治疗方法主要有肝切除术、肝移植术、栓塞化疗、消融疗法、化学疗法等。对于早期HCC患者,肝移植术较其他治疗方法能使患者获得更高的总生存率及无复发生存率[4]。因此,HCC肝移植术后不良情况的预测及肝移植术受体的选择非常重要。尽管目前可通过影像学指标、有无微血管侵犯等病理学指标、甲胎蛋白(AFP)等生物标志物预测HCC的复发,但这些指标灵敏度和特异度均不高。目前对于HCC复发的精准预测仍为临床难题。
中性粒细胞/淋巴细胞比值(NLR)是一种评估炎症反应程度的标志物,被广泛应用于感染性疾病、急性冠状动脉综合征、恶性肿瘤等疾病程度和预后的判断。NLR获取简便、检查费用低,大部分患者可以承担。已有多项研究发现NLR可用于预测HCC患者肝切除术后预后,如Yang等[5]的研究显示,术前外周血NLR升高提示该类患者总体生存率和无病生存率较低,且术前外周血高NLR为患者术后死亡的独立危险因素。然而,目前鲜见研究将NLR用于预测HCC患者移植术后预后。因此,本研究对HCC患者肝移植术前NLR水平对患者复发的影响进行探讨。
1 资料与方法 1.1 一般资料选择2017年1月至2020年12月于复旦大学附属中山医院肝肿瘤外科首次进行肝移植手术的患者278例。纳入标准:(1)符合《原发性肝癌诊疗指南(2022年版)》,经病理诊断为HCC;(2)2周内未使用抗生素;(3)患者及家属签署知情同意书。排除标准:(1)酒精性肝硬化;(2)肝内胆管细胞癌;(3)合并其他恶性肿瘤;(4)术前有急性或慢性感染。患者筛选流程见图 1。本研究获得复旦大学附属中山医院伦理委员会审批(B2022-435R)。

|
| 图 1 患者筛选入组流程 |
收集术前肝脏肿瘤分期、肿瘤分级、影像学指标、血清生物标志物及术后复发情况等临床病理资料。所有患者术前血常规指标、生化指标、凝血指标、肿瘤标志物血样均为术前3 d内采集。中性粒细胞绝对值、淋巴细胞绝对值和血小板计数(PLT)等血常规指标经Sysmex XN-9000全自动血液分析仪检测,计算NLR。凝血酶原时间(PT)经Sysmex CN-6000全自动凝血分析仪检测。血清乙型肝炎病毒表面抗原、丙型肝炎病毒抗体和AFP经Roche e801全自动电化学发光分析仪检测。白蛋白(Alb)、总胆红素(TBil)和丙氨酸氨基转移酶(ALT)经Roche c702全自动生化分析仪检测。无复发生存时间为患者肝移植手术后获得完全缓解到复发或随访截止时间。NLR为偏态分布,以75%分位数1.97将患者分为2组。
1.3 统计学处理采用IBM SPSS Statistics 26.0进行统计分析。采用K-S单样本检验确定研究指标的正态性,符合正态分布的计量资料以x±s表示,非正态分布的计量资料以M(P25, P75)表示。两组间比较采用独立样本t检验或K-S检验。计数资料以n(%)表示,两组间比较采用χ2检验。采用Kaplan-Meier生存曲线分析HCC患者肝移植手术后复发情况。采用单因素及多因素Cox回归分析评估复发危险因素。检验水准(α)为0.05。
2 结果 2.1 患者基线临床情况最终纳入149例HCC患者,其中男性125例,女性24例。NLR<1.97者38例(25.5%),NLR≥1.97者111例(74.5%)。结果(表 1)显示:两组间Child-Pugh分级、AFP和PT差异有统计学意义(P<0.05);两组间性别、年龄、乙肝史、丙肝史、肝硬化史等差异无统计学意义。
| 项目 | NLR<1.97 (n=38) | NLR≥1.97 (n=111) | P值 |
| 性别 | 0.199 | ||
| 男 | 29(76.3) | 96(86.5) | |
| 女 | 9(23.7) | 15(13.5) | |
| 年龄 | |||
| ≥60岁 | 21(55.3) | 46(41.4) | |
| <60岁 | 17(44.7) | 65(58.6) | |
| 乙肝病毒感染或乙肝病史 | 0.999 | ||
| 无 | 2(5.3) | 5(4.5) | |
| 有 | 36(94.7) | 106(95.5) | |
| 丙肝病毒感染或丙肝病史 | 0.999 | ||
| 无 | 38(100.0) | 110(99.1) | |
| 有 | 0 | 1(0.9) | |
| 肝硬化 | 0.185 | ||
| 无 | 1(2.6) | 12(10.8) | |
| 有 | 37(97.4) | 99(89.2) | |
| Child-Pugh分级 | 0.013 | ||
| A | 10(26.3) | 56(50.5) | |
| B+C | 28(73.7) | 55(49.5) | |
| AFP/(ng·mL-1) | 8.65(4.28, 52.98) | 69.10(5.40, 960.70) | 0.002 |
| ALT/(U·L-1) | 35.00(22.00, 45.75) | 41.00(30.00, 64.00) | 0.083 |
| Alb/(g·L-1) | 40.00(36.00, 43.00) | 40.00(35.00, 46.00) | 0.953 |
| PT/s | 13.25(12.10, 14.30) | 15.40(13.00, 18.20) | 0.001 |
| PLT/(×109·L-1) | 105.00(61.00, 146.75) | 84.00(52.00, 137.00) | 0.278 |
| TBil/(μmol·L-1) | 19.90(14.23, 27.85) | 24.50(16.00, 57.60) | 0.205 |
结果(表 2)显示:两组脉管侵犯比例、微脉管侵犯比例、BCLC分级及AJCC分期差异有统计学意义(P<0.05);两组患者肿瘤最大径、肿瘤数目等差异无统计学意义。
| 项目 | NLR<1.97 (n=38) | NLR≥1.97 (n=111) | P值 |
| 肿瘤最大径 | 0.074 | ||
| <5 cm | 30(78.9) | 69(62.2) | |
| ≥5 cm | 8(21.1) | 42(37.8) | |
| 肿瘤数目 | 0.699 | ||
| 单发 | 13(34.2) | 44(39.6) | |
| 多发 | 25(65.8) | 67(60.4) | |
| 肿瘤包膜 | 11(28.9) | 24(21.6) | 0.380 |
| 脉管侵犯 | 4(10.5) | 34(30.6) | 0.017 |
| 微脉管侵犯 | 16(42.1) | 84(75.7) | 0.001 |
| 播散灶 | 5(13.2) | 33(29.7) | 0.052 |
| BCLC分级 | 0.033 | ||
| 0+A级 | 20(52.6) | 36(32.4) | |
| B+C级 | 18(47.4) | 75(67.6) | |
| AJCC分期 | 0.023 | ||
| Ⅰ+Ⅱ期 | 27(71.1) | 54(48.6) | |
| Ⅲ期 | 11(28.9) | 57(51.4) |
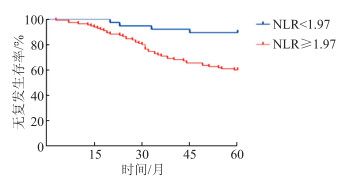
Kaplan-Meier生存曲线(图 2)显示:NLR<1.97组与NLR≥1.97组平均无复发生存时间分别为(56.87±1.57)、(48.00±1.62)个月,5年复发率分别为10.5%、39.6%。Log-rank检验结果显示两组患者无复发生存率差异有统计学意义(χ2=10.006,P=0.002)。
|
| 图 2 Kaplan-Meier生存曲线分析HCC患者肝移植术后复发情况 χ2=10.006, P=0.002 |
单因素Cox回归分析(表 3)显示:ALT、AFP、NLR,BCLC分级、AJCC分期,肿瘤最大径,脉管侵犯、微脉管侵犯、播散灶、肝硬化有无为HCC患者肝移植术后复发的影响因素(P<0.05)。多因素Cox回归分析(表 4)显示:BCLC分级为B级及以上、肿瘤最大径≥5 cm和NLR≥1.97为HCC患者肝移植术后复发的独立危险因素(P<0.05)。
| 因素 | HR(95%Cl) | P值 |
| 性别 | 2.309 (0.829~6.429) | 0.109 |
| 年龄 | 1.343 (0.753~2.396) | 0.317 |
| TBil (≥20.4 μmol/L vs<20.4 μmol/L) | 1.078 (0.607~1.078) | 0.797 |
| ALT (≥75 U/L vs<75 U/L) | 2.775 (1.488~5.175) | 0.001 |
| AFP (≥400 ng/mL vs<400 ng/mL) | 3.488 (1.976~6.156) | 0.001 |
| NLR (≥1.97 vs<1.97) | 4.494 (1.614~12.514) | 0.004 |
| Child-Pugh分级(B+C级vs A级) | 1.463 (0.830~2.577) | 0.188 |
| BCLC分级(B+C级vs 0+A级) | 4.337 (1.944~9.676) | 0.001 |
| AJCC分期(Ⅲ期vs Ⅰ+Ⅱ期) | 2.222 (1.237~3.990) | 0.008 |
| 肿瘤最大径(≥ 5 cm vs<5 cm) | 4.958 (2.736~8.986) | 0.001 |
| 肿瘤数目(多发vs 单发) | 1.765 (0.933~3.337) | 0.081 |
| 肿瘤包膜(有 vs无) | 0.780 (0.378~1.610) | 0.501 |
| 脉管侵犯(有vs 无) | 4.169 (2.359~7.370) | 0.001 |
| 微脉管侵犯(有 vs无) | 3.419 (1.533~7.627) | 0.003 |
| 播散灶(有vs无) | 2.980 (1.685~5.268) | 0.001 |
| 肝硬化(有 vs无) | 0.440 (0.197~0.982) | 0.045 |
| 因素 | HR (95%Cl) | P值 |
| BCLC分级(B+C级vs 0+A级) | 1.487 (1.094~2.019) | 0.011 |
| 肿瘤最大径(≥5 cm vs<5 cm) | 1.175 (1.106~1.248) | 0.001 |
| 肝硬化(有vs无) | 0.449 (0.188~1.076) | 0.073 |
| NLR (≥1.97 vs<1.97) | 3.611 (1.278~10.202) | 0.015 |
随着肝切除术、肝移植术、消融疗法及化疗等治疗手段的发展,HCC的疗效取得一定进步。De'Angelis等[6]研究显示,采用米兰标准筛选的HCC患者肝移植术后的平均复发率仍达16%,这是由于影像学不能精准预测肿瘤的大小、个数、分布、分级、分化及血管侵犯情况。除影像学指标外,目前临床上较为常用的HCC诊断及预后预测血清指标包括高尔基体跨膜糖蛋白73(golgiprotein 73,GP73)、AFP、甲胎蛋白异质体(LCA-bound fraction of AFP, AFP-L3)及α-L-岩藻糖苷酶(α-L-fucosidase,AFU)等。这些指标因无法达到灵敏度、特异度、准确度俱佳,临床应用均存在一定限制[7]。
人体炎症反应与恶性肿瘤的发生发展密切相关,炎性细胞所分泌的炎症介质及趋化因子可能加速恶性肿瘤细胞的增殖、转移,导致恶性肿瘤患者预后变差。同时,炎症反应使血液循环中中性粒细胞数目增多、淋巴细胞数目减少。中性粒细胞可通过分泌血管内皮生长因子(VEGF)促进肿瘤的增殖发展,而淋巴细胞具有抗肿瘤活性,因此NLR可作为系统性炎症标志物用于预测恶性肿瘤患者的预后[8]。
Miyamoto等[9]在154例胃癌患者中发现,NLR可以作为常规标志物的补充在胃癌患者的短期预后和长期预后预测中发挥作用;Moon等[10]在496例早期乳腺癌患者中发现,NLR可作为预测乳腺癌复发的独立影响因素。Lu等[11]发现,NLR对于早期或中期HCC(BCLC 0/A、B级)患者肝切除术后生存率有预测作用,并提出以2.81为NLR截断值。Da Fonseca等[12]在接受索拉非尼治疗的晚期HCC患者中发现NLR可预测患者生存率,并提出以3.5为NLR截断值。本研究通过Kaplan-Meier生存曲线发现,NLR≥1.97组的总体复发率高于NLR<1.97组(P=0.002),无复发生存时间短于NLR<1.97组。本研究截断值不同于文献报道,可能与HCC患者入组条件和治疗方案存在差异有关。本研究多因素Cox回归显示,BCLC分级为B级及以上、肿瘤最大径≥5 cm和NLR≥1.97为HCC患者肝移植术后复发的独立危险因素(P<0.05)。
综上所述,本研究提示,NLR可作为预测HCC患者肝移植术后复发的生物标志物,可作为影像学指标及传统生物标志物(AFP、CEA等)的补充与其联合使用,为临床选择合适的肝移植受体及预测肝移植术后预后提供参考。但本研究为单中心回顾性研究,样本量有限,患者入组过程存在一定偏倚,尤其NLR两组间例数差异较大。扩大样本量的多中心研究有助于验证本研究结论,相关肿瘤生物学机制也有待进一步探讨。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
KULIK L, EL-SERAG H B. Epidemiology and management of hepatocellular carcinoma[J]. Gastroenterology, 2019, 156(2): 477-491.
[DOI]
|
| [2] |
OTTINGER S, KLÖPPEL A, RAUSCH V, et al. Targeting of pancreatic and prostate cancer stem cell characteristics by Crambe crambe marine sponge extract[J]. Int J Cancer, 2012, 130(7): 1671-1681.
[DOI]
|
| [3] |
CHEN W Q, ZHENG R S, BAADE P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132.
[DOI]
|
| [4] |
LLOVET J M, KELLEY R K, VILLANUEVA A, et al. Hepatocellular carcinoma[J]. Nat Rev Dis Primers, 2021, 7(1): 6.
[DOI]
|
| [5] |
YANG H J, GUO Z, YANG Y T, et al. Blood neutrophil-lymphocyte ratio predicts survival after hepatectomy for hepatocellular carcinoma: a propensity score-based analysis[J]. World J Gastroenterol, 2016, 22(21): 5088-5095.
[DOI]
|
| [6] |
DE'ANGELIS N, LANDI F, CARRA M C, et al. Managements of recurrent hepatocellular carcinoma after liver transplantation: a systematic review[J]. World J Gastroenterol, 2015, 21(39): 11185-11198.
[DOI]
|
| [7] |
徐伟红, 姚怡婷, 曹华, 等. 血清GP73、AFP-L3、AFP及AFU检测在原发性肝癌诊断中的应用评价[J]. 中华检验医学杂志, 2016, 39(4): 262-266. XU W H, YAO Y T, CAO H, et al. Assessment of serum GP73, AFP-L3, AFP and AFU detection in the diagnosis of hepatocellular carcinoma[J]. Chin J Lab Med, 2016, 39(4): 262-266. [CNKI] |
| [8] |
MOTOMURA T, SHIRABE K, MANO Y, et al. Neutrophil-lymphocyte ratio reflects hepatocellular carcinoma recurrence after liver transplantation via inflammatory microenvironment[J]. J Hepatol, 2013, 58(1): 58-64.
[DOI]
|
| [9] |
MIYAMOTO R, INAGAWA S, SANO N, et al. The neutrophil-to-lymphocyte ratio (NLR) predicts short-term and long-term outcomes in gastric cancer patients[J]. Eur J Surg Oncol, 2018, 44(5): 607-612.
[DOI]
|
| [10] |
MOON G, NOH H, CHO I J, et al. Prediction of late recurrence in patients with breast cancer: elevated neutrophil to lymphocyte ratio (NLR) at 5 years after diagnosis and late recurrence[J]. Breast Cancer, 2020, 27(1): 54-61.
[DOI]
|
| [11] |
LU S D, WANG Y Y, PENG N F, et al. Preoperative ratio of neutrophils to lymphocytes predicts postresection survival in selected patients with early or intermediate stage hepatocellular carcinoma[J]. Medicine (Baltimore), 2016, 95(5): e2722.
[DOI]
|
| [12] |
DA FONSECA L G, BARROSO-SOUSA R, DA SILVA ALVES BENTO A, et al. Pre-treatment neutrophil-to-lymphocyte ratio affects survival in patients with advanced hepatocellular carcinoma treated with sorafenib[J]. Med Oncol, 2014, 31(11): 264.
[DOI]
|
 2022, Vol. 29
2022, Vol. 29


