2. 徐州医科大学附属医院神经内科, 徐州 221000
2. Department of Neurology, Affiliated Hospital of Xuzhou Medical University, Xuzhou 221000, Jiangsu, China
卒中已成为全世界致残和死亡的主要原因[1],尽管卒中的早期治疗策略不断完善,急性缺血性卒中(acute ischemic stroke,AIS)患者的预后仍不理想[2]。最近研究[3]表明,炎症反应和血脂异常在动脉粥样硬化病理生理的发生发展过程中起重要作用。单核细胞是白细胞的亚型,在缺血性中风后的急性期,通过与活化的内皮细胞上的黏附分子结合而渗入中枢神经系统,参与炎性损伤反应[4]。高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)通过逆转胆固醇转运并预防内皮功能障碍,产生抗凋亡、抗氧化、抗炎和抗血栓形成的作用,从而降低动脉粥样硬化事件的发生风险[5]。单核细胞与高密度脂蛋白胆固醇之比(monocyte to high-density lipoprotein cholesterol ratio,MHR)作为炎症和氧化应激的一种新兴指标,被认为可能是AIS患者功能预后不良重要且独立的预测指标[6-8]。本研究旨在评估急性缺血性卒中患者MHR与3个月功能预后之间的关系,以更好地识别出不良结果风险较高患者,进行进一步的潜在干预。
1 资料与方法 1.1 研究对象回顾性收集2019年7月至2020年9月海军军医大学第二附属医院神经内科住院收治的AIS患者313例,根据患者的病史、临床特征和神经影像表现(计算机体层扫描或磁共振成像)、世界卫生组织定义的标准[9]对AIS进行了诊断。本研究获得海军军医大学第二附属医院伦理委员会批准(2019061210),所有患者均知情且签署知情同意书。
纳入标准:(1)首次中风发作且为确诊的缺血性中风患者;(2)中风发作后36 h内抽血。排除标准:(1)从发病到入院的时间超过48 h;(2)无完整临床资料的患者;(3)有癌症病史、使用免疫抑制剂或血液系统疾病;(4)严重的肝、肾疾病;(5)重大外伤、手术或失访;(6)慢性炎性疾病或慢性感染或中风前的免疫系统疾病。
1.2 观察指标收集患者的一般临床资料。人口统计学特征包括年龄、性别、吸烟史、饮酒史、他汀类药物使用史、入院收缩压及舒张压。血管危险因素包括高血压、糖尿病、心房颤动、高脂血症病史。采用美国国立卫生研究院卒中量表(NIHSS)评估AIS患者入院后24 h内神经系统损害的基线严重程度。
入院后24 h内常规进行实验室检查,包括白细胞、中性粒细胞、淋巴细胞、单核细胞、空腹血糖、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、尿酸、同型半胱氨酸(homocysteine,Hcy)、神经元特异烯醇化酶(neuronspecific enolase,NSE)。
1.3 分组与随访根据改良的Rankin量表(mRS)评估了AIS患者的功能预后,分为良好预后组(mRS≤2,n=260)和不良预后组(mRS>2,n=53)。3个月后,通过门诊对每个参与者进行了随访。
1.4 统计学处理采用SPSS 25.0软件进行统计分析,计量资料以x±s表示,采用独立样本t检验;计数资料以n(%)表示,采用χ2检验或Fisher精确检验。采用多因素logistic回归分析以评估单核细胞、HDL-C、MHR与AIS患者3个月预后之间的关系。采用ROC曲线分析评估单核细胞、HDL-C、MHR对AIS患者预后的预测价值。检验水准(α)为0.05。
2 结果 2.1 一般资料分析结果(表 1)显示:与良好预后组相比,不良预后组的入院NIHSS评分更高[(3.39±3.36)vs (10.04±4.66),P < 0.001],年龄、男性、他汀使用史、高血压、糖尿病、吸烟史、饮酒史差异有统计学意义(P < 0.05)。不良预后组的白细胞、中性粒细胞、单核细胞、空腹血糖、尿酸、TG、HDL-C、Hcy、NSE与良好预后组相比差异有统计学意义(P < 0.05);且较高的MHR[(4.10±0.62) vs (5.25±0.85),P < 0.001]与AIS患者不良预后独立相关。但2组间的房颤史、高脂血症史、入院收缩压、入院舒张压、TC、LDL-C差异无统计学意义。
| 指标 | 良好预后组(n=260) | 不良预后组(n=53) | t/χ2值 | P值 |
| 男性n(%) | 155(59.6) | 40(75.5) | 4.713 | 0.030 |
| 年龄/岁 | 66.78±9.25 | 78.11±6.87 | 10.263 | < 0.001 |
| 他汀使用史n(%) | 79(30.4) | 9(17.0) | 3.913 | 0.048 |
| 高血压n(%) | 185(71.2) | 47(88.7) | 7.049 | 0.008 |
| 糖尿病n(%) | 80(30.8) | 32(60.4) | 16.796 | < 0.001 |
| 房颤n(%) | 16(6.2) | 7(13.2) | 2.265 | 0.132 |
| 高脂血症n(%) | 78(30.0) | 11(20.8) | 1.849 | 0.174 |
| 吸烟史n(%) | 108(41.5) | 11(20.8) | 8.070 | 0.004 |
| 饮酒史n(%) | 84(32.3) | 10(18.9) | 3.784 | 0.052 |
| 入院收缩压/mmHg | 134.62±21.06 | 137.94±20.36 | 1.053 | 0.293 |
| 入院舒张压/mmHg | 83.46±10.16 | 83.98±10.93 | 0.337 | 0.736 |
| NIHSS评分 | 3.39±3.36 | 10.04±4.66 | 9.883 | < 0.001 |
| 白细胞(×109/L) | 6.85±1.20 | 7.69±1.05 | 4.756 | < 0.001 |
| 中性粒细胞(×109/L) | 4.23±1.07 | 5.18±1.09 | 5.886 | < 0.001 |
| 淋巴细胞(×109/L) | 1.71±0.37 | 1.47±0.29 | -5.240 | < 0.001 |
| 单核细胞(×108/L) | 4.44±0.68 | 5.40±0.87 | 7.568 | < 0.001 |
| 空腹血糖/(mmol·L-1) | 6.12±2.06 | 7.08±2.57 | 2.948 | 0.003 |
| 尿酸/(μmol·L-1) | 338.98±97.48 | 369.79±68.95 | 2.743 | 0.007 |
| TC/(mmol·L-1) | 4.73±0.97 | 4.56±0.88 | -1.170 | 0.243 |
| TG/(mmol·L-1) | 2.07±0.57 | 1.26±0.47 | -10.924 | < 0.001 |
| HDL-C/(mmol·L-1) | 1.09±0.11 | 1.03±0.10 | -3.387 | 0.001 |
| LDL-C/(mmol·L-1) | 2.68±0.70 | 2.83±0.60 | 1.407 | 0.160 |
| Hcy/(μmol·L-1) | 13.59±4.07 | 16.88±5.22 | 4.328 | < 0.001 |
| NSE/(μg·L-1) | 13.26±3.85 | 17.02±4.37 | 6.336 | < 0.001 |
| MHR | 4.10±0.62 | 5.25±0.85 | 9.312 | < 0.001 |
| NIHSS:美国国立卫生研究院卒中量表;TC:总胆固醇;TG:三酰甘油;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;Hcy:同型半胱氨酸;NSE:神经元特异烯醇化酶;MHR:单核细胞与高密度脂蛋白胆固醇之比。 | ||||
结果(表 2)显示:男性、NIHSS评分高、年龄较大者,有高血压病史、糖尿病病史、吸烟史者,且尿酸、同型半胱氨酸、白细胞、单核细胞、MHR升高,TG、HDL-C降低均为影响AIS患者预后的危险因素。
| 自变量 | OR(95%CI) | P值 | 自变量 | OR(95%CI) | P值 | ||
| 男性 | 2.084(1.063~4.086) | 0.032 | NIHSS评分 | 1.419(1.298~1.551) | < 0.001 | ||
| 年龄 | 1.176(1.122~1.233) | < 0.001 | 尿酸 | 1.003(1.000~1.006) | 0.032 | ||
| 他汀使用史 | 0.469(0.218~1.006) | 0.052 | Hcy | 1.161(1.090~1.237) | < 0.001 | ||
| 高血压 | 3.176(1.303~7.741) | 0.011 | TG | 0.048(0.021~0.113) | < 0.001 | ||
| 糖尿病 | 3.429(1.863~6.311) | < 0.001 | 白细胞 | 1.881(1.421~2.489) | < 0.001 | ||
| 房颤 | 2.321(0.904~5.955) | 0.080 | 单核细胞 | 4.699(3.027~7.295) | < 0.001 | ||
| 高脂血症 | 0.611(0.299~1.249) | 0.177 | HDL-C | 0.007(0.000~0.137) | 0.001 | ||
| 吸烟史 | 0.369(0.182~0.748) | 0.006 | MHR | 8.282(4.780~14.350) | < 0.001 | ||
| 饮酒史 | 0.487(0.234~1.017) | 0.055 | |||||
| NIHSS:美国国立卫生研究院卒中量表;TC:总胆固醇;TG:三酰甘油;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;Hcy:同型半胱氨酸;NSE:神经元特异烯醇化酶;MHR:单核细胞与高密度脂蛋白胆固醇之比。 | |||||||
结果(表 3、表 4)显示:年龄、NIHSS评分、TG、MHR是影响AIS患者3个月预后情况的独立危险因素。高MHR(OR=2.690,95%CI 1.017~7.111,P=0.046)、年龄较大者、NIHSS评分高、低TG与3个月后不良预后仍显著相关;而在单核细胞(OR=2.046,95%CI 0.764~5.478,P=0.154)、HDL-C(OR=0.001,95%CI 0.000~1.060,P=0.052)中并未发现此联系。
| 自变量 | OR(95%CI) | P值 |
| 男性 | 1.645(0.434~6.232) | 0.464 |
| 年龄 | 1.224(1.112~1.349) | < 0.001 |
| 他汀使用史 | 0.253(0.058~1.106) | 0.068 |
| 高血压 | 0.298(0.060~1.487) | 0.140 |
| 糖尿病 | 0.593(0.173~2.039) | 0.407 |
| 房颤 | 0.387(0.075~1.997) | 0.257 |
| 高脂血症 | 0.929(0.236~3.651) | 0.916 |
| 吸烟史 | 0.718(0.133~3.866) | 0.700 |
| 饮酒史 | 0.947(0.170~5.281) | 0.950 |
| NIHSS评分 | 1.542(1.297~1.832) | < 0.001 |
| 尿酸 | 1.004(0.998~1.009) | 0.203 |
| Hcy | 1.062(0.933~1.208) | 0.364 |
| TG | 0.220(0.054~0.885) | 0.033 |
| 白细胞 | 1.154(0.647~2.057) | 0.629 |
| MHR | 2.690(1.017~7.111) | 0.046 |
| NIHSS:美国国立卫生研究院卒中量表;TG:甘油三酯;Hcy:同型半胱氨酸;MHR:单核细胞与高密度脂蛋白胆固醇之比。 | ||
| 自变量 | OR(95%CI) | P值 |
| 男性 | 1.569(0.413~5.954) | 0.508 |
| 年龄 | 1.229(1.115~1.355) | < 0.001 |
| 他汀使用史 | 0.252(0.057~1.104) | 0.067 |
| 高血压 | 0.353(0.072~1.745) | 0.202 |
| 糖尿病 | 0.620(0.177~2.168) | 0.454 |
| 房颤 | 0.338(0.062~1.857) | 0.212 |
| 高脂血症 | 1.125(0.267~4.743) | 0.872 |
| 吸烟史 | 0.620(0.112~3.433) | 0.584 |
| 饮酒史 | 0.974(0.174~5.472) | 0.976 |
| NIHSS评分 | 1.534(1.293~1.820) | < 0.001 |
| 尿酸 | 1.004(0.998~1.010) | 0.151 |
| Hcy | 1.062(0.932~1.210) | 0.369 |
| TG | 0.211(0.053~0.847) | 0.028 |
| 白细胞 | 1.312(0.707~2.436) | 0.390 |
| 单核细胞 | 2.046(0.764~5.478) | 0.154 |
| HDL-C | 0.001(0.000~1.060) | 0.052 |
| NIHSS:美国国立卫生研究院卒中量表;TG:甘油三酯;Hcy:同型半胱氨酸;HDL-C:高密度脂蛋白胆固醇。 | ||
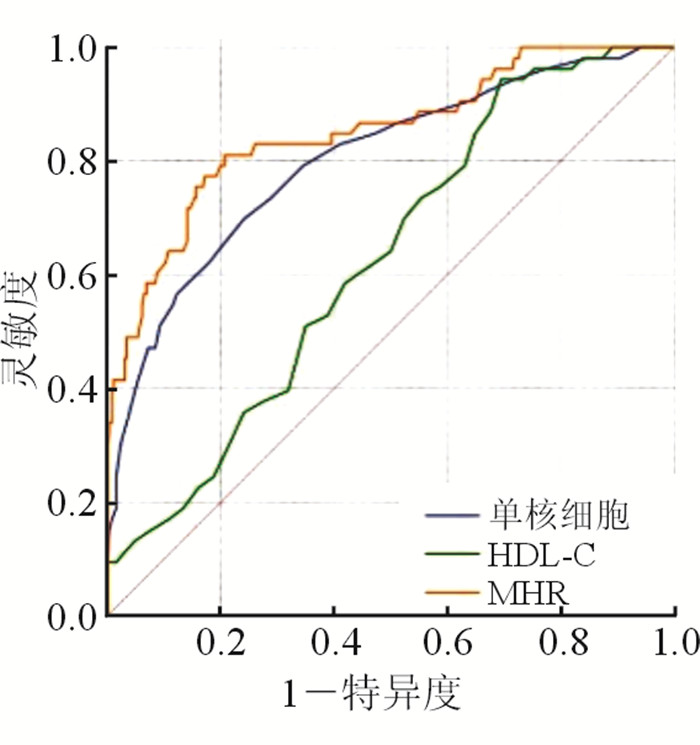
结果(表 5、图 1)显示:MHR预测AIS患者3个月不良预后的效果最佳,根据约登指数,最佳预测截断值为4.580,灵敏度81.1%,特异度79.2%。MHR的AUC为0.851(95%CI 0.788~0.913,P < 0.001)高于单核细胞0.802(95%CI 0.733~0.870,P < 0.001)和HDL-C 0.627(95%CI 0.552~0.702,P=0.004)。
| 指标 | AUC(95%CI) | P值 | 截断值 | 灵敏度/% | 特异度/% |
| MHR | 0.851 (0.788~0.913) |
< 0.001 | >4.580 | 81.1 | 79.2 |
| 单核细胞 | 0.802 (0.733~0.870) |
< 0.001 | >4.850 | 69.8 | 75.8 |
| HDL-C | 0.627 (0.552~0.702) |
0.004 | < 1.155 | 30.4 | 94.3 |
| AUC:曲线下面积;CI:置信区间;MHR:单核细胞与高密度脂蛋白胆固醇之比;HDL-C:高密度脂蛋白胆固醇。 | |||||
|
| 图 1 单核细胞、HDL-C、MHR对AIS患者预后的ROC曲线 |
本研究中,单因素分析显示,单核细胞、HDL-C、MHR是影响AIS患者3个月预后的危险因素;在多因素分析中,MHR仍显著,而单核细胞、HDL-C并未发现此关联。此外,不良预后的患者年龄较大、NIHSS评分较高、而TG较低。同时,通过ROC曲线分析得出,MHR预测AIS患者3个月预后情况的价值最大,最佳预测截断值为4.580。
越来越多的证据[3-4]表明,免疫炎性反应和氧化应激在中风中发挥着重要作用。单核细胞作为白细胞的一种特殊亚型,可在急性脑缺血发作后的4 h内出现组织浸润,7 d后达高峰[10]。在氧化的低密度脂蛋白(ox-LDL)的刺激下,单核细胞黏附于内皮细胞并分化为巨噬细胞,通过产生各种类型的促炎和促氧化介质渗透黏附到动脉壁内并与内皮细胞相互作用,通过吞噬ox-LDL和其他脂质而导致炎症级联反应和泡沫细胞形成,继而演变成动脉粥样硬化或动脉粥样硬化斑块[11-12]。单核细胞趋化蛋白-1(monocyte chemoattractant protein-1,MCP-1)的过表达通过募集包括白细胞介素-6(interleukin-6,IL-6)、白细胞介素-1β(interleukin-1β,IL-1β)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)等促炎细胞因子和粒细胞集落刺激因子在内的炎症细胞而加剧了脑损伤[13]。有研究[14]表明,单核细胞和血浆MCP-1水平可以作为早期AIS患者疾病严重程度的临床预后指标。另一项研究[15]发现,卒中后的不良结局和死亡率增加以及早期临床功能恶化与中风后48 h CD14++/CD16+单核细胞达到峰值的比例增加有关。ox-LDL引起的单核细胞迁移是由于MCP-1合成的诱导,而HDL和抗氧化剂可防止LDL诱导的单核细胞迁移[16]。相反,HDL-C通过抑制细胞CD11b的活化表现出对人单核细胞的抗炎作用[17]。HDL还通过增加血管中NO的生物利用度来促进内皮修复和抗血栓形成[18]。因此,HDL-C具有抗炎和抗氧化剂以及抗血栓形成作用[5]。
单核细胞的促炎作用,HDL-C的抗炎功能,使得MHR作为一种新的炎性标志物,能更好地预测心脑血管病及其他炎性疾病的预后。有研究[19]指出,MHR可能在细胞增殖、巨噬细胞趋化、中性粒细胞渗出、氧化应激等过程中发挥作用。另有研究[19-20]发现,MHR可能通过激活巨噬细胞炎症介质的释放促进泡沫细胞的形成,也可能通过抑制平滑肌细胞与基质的粘附等过程影响动脉粥样硬化斑块的形成和发展。MHR作为一种综合性的炎症因子,比单核细胞或HDL-C计数更加稳定,且在临床工作中容易获得,是全身性炎症和内皮功能障碍的替代标志。
最近的研究[6, 19, 21]发现,MHR可能是AIS患者不良预后重要且独立的预测指标。Bolayir等[22]指出,较高的MHR值可预测AIS患者30 d的死亡率。一项荟萃分析[23]发现,接受原发性经皮冠状动脉介入治疗的ST抬高型心肌梗死患者中较高的MHR入院率与更高的院内死亡率和主要不良心血管事件有关。入院时较高的MHR可预测AIS患者的中风相关性肺炎,但与3个月全因死亡率之间无显著相关性[24]。较高的MHR与急性脑出血患者出院时和3个月后致残或死亡的风险增加相关[25]。
本研究也存在一些不足:(1)样本量较少,男女比例相差较大,且患者均来自同一家医院,不可避免地存在选择偏倚;(2)实验室数据只收集了1次,没有动态监测,缺乏准确性。因此,未来需要更多的前瞻性研究。
综上所述,MHR作为全身炎症性疾病和氧化应激有用的预后标志物,是预测缺血性中风预后的独立预测因子。在临床实践中,MHR作为一种新型炎症标志物,是一种简单、经济、可重复的临床工具,可能为临床工作中判断患者预后提供一个方便可行的参考依据,并且可能是中风治疗的新靶点,在临床工作中将两者结合,在预测卒中预后的效用方面将大大提高,有助于及早发现高危患者,以提供及时的治疗干预及临床指导。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
ZERNA C, THOMALLA G, CAMPBELL B C V, et al. Current practice and future directions in the diagnosis and acute treatment of ischaemic stroke[J]. Lancet, 2018, 392(10154): 1247-1256.
[DOI]
|
| [2] |
PANDIAN J D, GALL S L, KATE M P, et al. Prevention of stroke: a global perspective[J]. Lancet, 2018, 392(10154): 1269-1278.
[DOI]
|
| [3] |
LIBBY P. Inflammation in atherosclerosis[J]. Arterioscler Thromb Vasc Biol, 2012, 32(9): 2045-2051.
[DOI]
|
| [4] |
KIM J Y, PARK J, CHANG J Y, et al. Inflammation after ischemic stroke: the role of leukocytes and glial cells[J]. Exp Neurobiol, 2016, 25(5): 241-251.
[DOI]
|
| [5] |
EREN E, ELLIDAG H Y, AYDIN O, et al. HDL functionality and crystal-based sterile inflammation in atherosclerosis[J]. Clin Chim Acta, 2015, 439: 18-23.
[DOI]
|
| [6] |
LIU H B, LIU K, PEI L L, et al. Monocyte-to-high-density lipoprotein ratio predicts the outcome of acute ischemic stroke[J]. J Atheroscler Thromb, 2020, 27(9): 959-968.
[DOI]
|
| [7] |
DENG Q W, WANG H, SUN C Z, et al. Triglyceride to high-density lipoprotein cholesterol ratio predicts worse outcomes after acute ischaemic stroke[J]. Eur J Neurol, 2017, 24(2): 283-291.
[DOI]
|
| [8] |
DENG Q W, LI S, WANG H, et al. The short-term prognostic value of the triglyceride-to-high-density lipoprotein cholesterol ratio in acute ischemic stroke[J]. Aging Dis, 2018, 9(3): 498-506.
[DOI]
|
| [9] |
Stroke——1989. Recommendations on stroke prevention, diagnosis, and therapy. Report of the WHO Task Force on Stroke and Other Cerebrovascular Disorders[J]. Stroke, 1989, 20(10): 1407-1431.
[DOI]
|
| [10] |
GARCIA J H, LIU K F, YOSHIDA Y, et al. Influx of leukocytes and platelets in an evolving brain infarct (Wistar rat)[J]. Am J Pathol, 1994, 144(1): 188-199.
|
| [11] |
GEISSMANN F, JUNG S, LITTMAN D R. Blood monocytes consist of two principal subsets with distinct migratory properties[J]. Immunity, 2003, 19(1): 71-82.
[DOI]
|
| [12] |
GEISSMANN F, MANZ M G, JUNG S, et al. Development of monocytes, macrophages, and dendritic cells[J]. Science, 2010, 327(5966): 656-661.
[DOI]
|
| [13] |
STRECKER J K, MINNERUP J, GESS B, et al. Monocyte chemoattractant protein-1-deficiency impairs the expression of IL-6, IL-1β and G-CSF after transient focal ischemia in mice[J]. PLoS One, 2011, 6(10): e25863.
[DOI]
|
| [14] |
VIEDT C, ORTH S R. Monocyte chemoattractant protein-1(MCP-1) in the kidney: does it more than simply attract monocytes?[J]. Nephrol Dial Transplant, 2002, 17(12): 2043-2047.
[DOI]
|
| [15] |
URRA X, VILLAMOR N, AMARO S, et al. Monocyte subtypes predict clinical course and prognosis in human stroke[J]. J Cereb Blood Flow Metab, 2009, 29(5): 994-1002.
[DOI]
|
| [16] |
NAVAB M, IMES S S, HAMA S Y, et al. Monocyte transmigration induced by modification of low density lipoprotein in cocultures of human aortic wall cells is due to induction of monocyte chemotactic protein 1 synthesis and is abolished by high density lipoprotein[J]. J Clin Invest, 1991, 88(6): 2039-2046.
[DOI]
|
| [17] |
ANSELL B J, NAVAB M, HAMA S, et al. Inflammatory/antiinflammatory properties of high-density lipoprotein distinguish patients from control subjects better than high-density lipoprotein cholesterol levels and are favorably affected by simvastatin treatment[J]. Circulation, 2003, 108(22): 2751-2756.
[DOI]
|
| [18] |
TABET F, RYE K A. High-density lipoproteins, inflammation and oxidative stress[J]. Clin Sci (lond), 2009, 116(2): 87-98.
[DOI]
|
| [19] |
GANJALI S, JRGOTTO A M, RUSCICA M, et al. Monocyte-to-HDL-cholesterol ratio as a prognostic marker in cardiovascular diseases[J]. J Cell Physiol, 2018, 233(12): 9237-9246.
[DOI]
|
| [20] |
YILMAZ M, KAYANÇIÇEK H. A new inflammatory marker: elevated monocyte to HDL cholesterol ratio associated with smoking[J]. J Clin Med, 2018, 7(4): 76.
[DOI]
|
| [21] |
KANBAY M, SOLAK Y, UNAL H U, et al. Monocyte count/HDL cholesterol ratio and cardiovascular events in patients with chronic kidney disease[J]. Int Urol Nephrol, 2014, 46(8): 1619-1625.
[DOI]
|
| [22] |
BOLAYIR A, GOKCE S F, CIGDEM B, et al. Monocyte/high-density lipoprotein ratio predicts the mortality in ischemic stroke patients[J]. Neurol Neurochir Pol, 2018, 52(2): 150-155.
[DOI]
|
| [23] |
VILLANUEVA D L E, TIONGSON M D, RAMOS J D, et al. Monocyte to high-density lipoprotein ratio (MHR) as a predictor of mortality and major adverse cardiovascular events (MACE) among ST elevation myocardial infarction (STEMI) patients undergoing primary percutaneous coronary intervention: a meta-analysis[J]. Lipids Health Dis, 2020, 19(1): 55.
[DOI]
|
| [24] |
SUN Y M, LU J, ZHENG D N, et al. Predictive value of monocyte to HDL cholesterol ratio for stroke-associated pneumonia in patients with acute ischemic stroke[J]. Acta Neurol Belg, 2020. Online ahead of print.
|
| [25] |
YOU S J, ZHONG C K, ZHENG D N, et al. Monocyte to HDL cholesterol ratio is associated with discharge and 3-month outcome in patients with acute intracerebral hemorrhage[J]. J Neurol Sci, 2017, 372: 157-161.
[DOI]
|
 2021, Vol. 28
2021, Vol. 28


