肝硬化引起的门脉高压症最严重的并发症主要有食管胃底静脉曲张破裂出血(esophageal and gastric varices bleeding, EGVB)和脾功能亢进。尽管EGVB的非手术治疗已获得长足发展,但其术后6周死亡率仍达20%[1-2],而非手术治疗后,较高的再出血率及脾功能亢进症状均严重影响患者的生活质量。因此,手术干预目前仍是治疗门静脉高压症患者EGVB和脾功能亢进首选方法。断流术是国内目前治疗EGVB最主要的手术方式[3],但各种术式的优劣势仍存在争议[4-5]。现回顾性分析南通大学附属医院2005年9月1日至2019年12月1日诊治的门脉高压症EGVB患者的临床资料,比较改良Sugiura术及选择性断流术对该类患者的有效性及安全性。
1 资料与方法 1.1 一般资料回顾性分析2005年9月1日至2019年12月1日在南通大学附属医院接受手术的215例门脉高压症EGVB患者的临床资料,根据纳入、排除标准入选改良Sugiura术组(改良组)45例、选择性断流术(选择组)65例(图 1)。其中,男性71例、女性39例,平均(55.11±9.32)岁。Child分级:A级74例,B级36例。食管静脉曲张程度根据2016年发布的《肝硬化门静脉高压食管胃静脉曲张出血的防治指南》判断:中度62例,重度48例。出血情况:术前半年内出血1~ 4次,至1 000 mL以上出血(黑便)。肝硬化原因:91例有慢性乙型肝炎病史, 余依次为血吸虫性、丙肝、酒精性及不明原因等。本研究经医院伦理委员会审核批准。

|
| 图 1 研究人群纳入、排除流程图 |
(1) 入院诊断为肝硬化、门脉高压症、脾肿大且伴有脾功能亢进;(2)既往有上消化道出血病史,且通过内镜证实,有中、重度食管胃底静脉曲张;(3)签署知情同意书。
1.2.2 排除标准(1) 急诊手术;(2)伴有严重影响生存时间的心、肺、肾等脏器功能不全、恶性肿瘤及血液系统疾病等;(3)美国麻醉医师协会(American Society of Anesthesiologists, ASA)评估Ⅲ级及以上;(4)术前Child分级为C级;(5)临床资料不全。
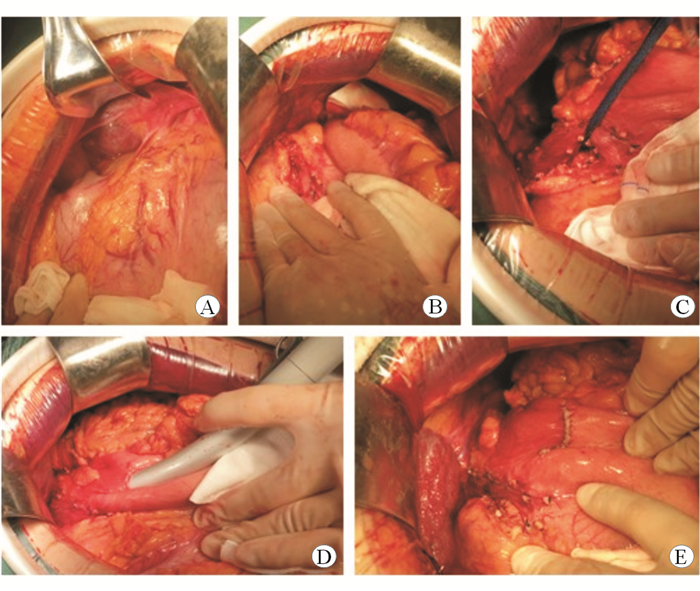
1.3 手术方法 1.3.1 选择性断流术全麻下经左侧腹直肌切口进腹,暴露脾脏后切除(图 2A),从胃体中部开始向上,紧贴胃、食管壁切断和结扎胃大、小弯侧、贲门周围及食管下段6~8 cm所有进入胃壁和食管壁的血管(图 2B)。注意保留冠状静脉主干,仅切断、结扎其进入胃及食管的分支;保留食管旁静脉(图 2C)。保留已形成侧支循环的腹壁、腹膜后静脉。缝合胃大、小弯侧前后壁浆膜,使其浆膜化,左膈下放置引流管。
|
| 图 2 选择性断流术及改良Sugiura手术过程 A:暴露脾脏;B:切脾后行胃大、小弯侧血管离断、结扎;C:悬吊食管,切断食管旁穿支静脉,仅保留胃冠状及食管旁静脉;D:切开胃体部,置入管型吻合器;E:关闭胃壁切口,加强吻合 |
进腹、切脾及断流均同选择性断流术。游离食管过程中, 切断迷走神经干。在距贲门约8 cm处切开胃体前壁,胃体前壁置入吻合器(图 2D),在贲门上方4~5 cm处用7号丝线将食管壁捆扎在吻合器主体与砧体之间,旋紧后击发吻合器,切除一小段食管壁并同时吻合。常规放置营养管于吻合口下至空肠10 cm处,用闭合器关闭胃壁切口(图 2E)。左膈下放置引流管,关腹。
1.4 术后处理术后给予止血、抗感染、及时输血及补充白蛋白。监测患者术后血常规及肝功能,当已无外科出血风险且血小板超过正常上限时,及时使用低分子肝素钙5 000 U/d皮下注射和阿司匹林口服抗凝至血小板基本恢复正常。
1.5 观察指标(1) 围术期指标:手术时间、术中出血量、术后住院时间、术后Clavien-Dindo分级等;(2)近、远期生存情况:术后近期(3个月内)死亡率、累计1、3、5年生存率;(3)食管胃底静脉曲张缓解率:术后3~6个月、1年及至随访截止日(2019年12月1日);(4)累计再出血率:1、3、5年及至随访截止日;(5)术前及术后门静脉系统重建情况:CT观察门静脉直径、食管胃底静脉曲张缓解情况以及门静脉血栓形成情况。
1.6 统计学处理所有病例资料数据录入Excel表,采用SPSS 25.0软件进行统计分析。计数资料以n(%)表示,组间比较采用χ2检验(Pearson卡方、连续校正的卡方及Fisher精确检验)分析;计量资料以x±s表示,组间比较采用t检验。采用Kaplan-Meier法分析总体生存率,组间比较log-rank检验。食管胃底静脉曲张缓解与否、再出血与否、及门静脉直径失访值采用多重填补法填补,检验水准(α)为0.05。
2 结果 2.1 基线情况结果(表 1)显示:两组患者性别、年龄、术前ASA分级、食管胃底静脉曲张程度、术前出血情况、Child分级及血常规等指标差异均无统计学意义。
| 指标 | 改良组(n=45) | 选择组(n=65) | χ2/ t值 | P值 |
| 性别n(%) | 0.688 | 0.407 | ||
| 男 | 27(60.00) | 44(67.69) | ||
| 女 | 18(40.00) | 21(32.31) | ||
| 年龄n(%) | 0.086 | 0.769 | ||
| ≥50岁 | 33(73.33) | 46(70.77) | ||
| <50岁 | 12(26.66) | 19(29.23) | ||
| ASA分级n(%) | 0.238 | 0.626 | ||
| Ⅰ | 38(84.44) | 57(87.69) | ||
| Ⅱ | 7(15.56) | 8(12.31) | ||
| BMI n(%) | 0.026 | 0.871 | ||
| 标准 | 27(60.00) | 40(61.54) | ||
| 非标准 | 18(40.00) | 25(38.46) | ||
| 食管胃底静脉曲张n(%) | 0.409 | 0.522 | ||
| 中 | 27(60.00) | 35(53.85) | ||
| 重 | 18(40.00) | 30(46.15) | ||
| 乙型肝炎肝硬化n(%) | 0.396 | 0.529 | ||
| 是 | 36(80.00) | 55(84.62) | ||
| 否 | 9(20.00) | 10(15.38) | ||
| 术前出血次数n(%) | 2.942 | 0.230 | ||
| 1次 | 21(46.67) | 21(32.31) | ||
| 2次 | 17(37.78) | 35(53.85) | ||
| ≥3次 | 7(15.56) | 9(13.85) | ||
| 出血量n(%) | 1.679 | 0.432 | ||
| 低 | 5(11.11) | 11(16.92) | ||
| 中 | 29(64.44) | 34(52.31) | ||
| 高 | 11(24.44) | 20(30.77) | ||
| Child分级n(%) | 1.830 | 0.176 | ||
| A | 27(60.00) | 47(72.31) | ||
| B | 18(40.00) | 18(27.69) | ||
| ALB/(g·L-1) | 31.27±2.69 | 30.41±20.32 | 1.690 | 0.094 |
| TBIL/(μmol·L-1) | 21.00±8.58 | 21.94±7.60 | -0.505 | 0.614 |
| PT/s | 13.83±1.95 | 13.93±2.28 | -0.333 | 0.740 |
| WBC/(×109·L-1) | 4.92±2.25 | 5.24±2.62 | -0.850 | 0.397 |
| PLT/(×109·L-1) | 62.33±16.50 | 58.19±18.07 | 0.925 | 0.357 |
| ASA: 美国麻醉医师协会分级;BMI: 体质量指数;ALB: 白蛋白;TBIL: 总胆红素;PT:凝血酶原时间;WBC:白细胞计数:PLT:血小板计数 | ||||
结果(表 2)显示:两组手术时间及术中出血量差异有统计学意义(P<0.05);两组术后住院天数、手术相关并发症发生率差异均无统计学意义。改良组无吻合口瘘、吻合口出血的发生,术后7例患者短期内进食时有哽咽感。其中5例于术后1个月内自行缓解;另2例哽咽症状持续达2个月,经多次胃镜球囊扩张后缓解,随访期内未再反复。
| 指标 | 改良组(n=45) | 选择组(n=65) | χ2/ t值 | P值 |
| 手术时间/min | 186.56±36.72 | 156.77±38.80 | 3.885 | < 0.001 |
| 术中出血量/mL | 307.70±69.05 | 279.46±72.67 | 2.050 | 0.043 |
| 术后住院天数 | 11.96±4.06 | 10.97±3.47 | 1.539 | 0.127 |
| Clavien-Dindo分级n(%) | 3.395 | 0.183 | ||
| Ⅰ | 17(37.78) | 22(33.85) | ||
| Ⅱ | 20(44.44) | 38(58.46) | ||
| Ⅲ | 8(17.78) | 5(7.69) | ||
| 术后并发症n(%) | ||||
| 顽固性腹水 | 5(11.11) | 8(12.31) | 0.037 | 0.848 |
| 门静脉血栓形成 | 3(6.67) | 6(9.23) | 0.017 | 0.898 |
| 胸腔积液 | 4(8.89) | 8(12.31) | 0.065 | 0.799 |
| 腹腔出血 | 3(6.67) | 2(3.08) | 0.179 | 0.672 |
| 膈下感染 | 3(6.67) | 3(4.62) | 0.002 | 0.969 |
| 肝性脑病 | 2(4.44) | 1(1.54) | 0.105 | 0.745 |
| 上消化道出血* | 1(2.22) | 1(1.54) | — | 1.000 |
| 吻合口狭窄* | 2(4.44) | 0(0.00) | — | 0.165 |
| * Fisher精确检验. Clavien-Dindo分级:手术并发症严重程度分级 | ||||
改良组术后近期发生再出血1例(2.22%);死亡1例(2.22%),死亡原因为腹腔感染合并多器官功能衰竭。选择组术后近期发生再出血2例(3.08%);死亡1例(1.54%),死亡原因为腹腔广泛渗血致弥散性血管内凝血(disseminated intravascular coagulation, DIC)。两组术后近期再出血率与死亡率差异无统计学意义。
2.3 随访及生存分析改良组随访41例(91.11%),随访时间6个月~10年,平均随访(4.33±2.94)年,累计1、3、5年生存率分别为97.14%、84.62%、78.26%;死亡原因:肝功能衰竭2例,原发性肝癌1例,直肠癌1例,术后抑郁症1例和腹腔感染合并多器官功能衰竭1例。选择组随访56例(86.15%),随访5个月~13年,平均随访(4.43±3.33)年,累计1、3、5年生存率分别为98.00%、89.19%、71.43%;死亡原因:肝功能衰竭3例,原发性肝癌2例,上消化道再出血2例,肺部感染致肺功能衰竭1例和腹腔广泛渗血致DIC 1例。
两组患者共完成随访97例,失访13例(11.82%)。失访原因:11例(84.62%)拒绝随访,2例(15.38%)无法联系。结果(图 3)显示:两组术后总生存率差异无统计学意义。

|
| 图 3 Kaplan-Meier生存分析 P=0.561 |
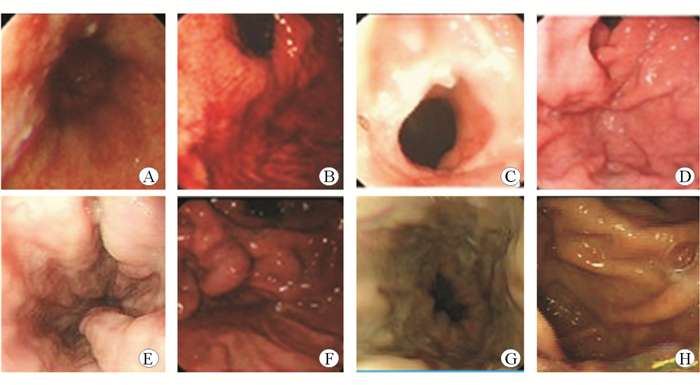
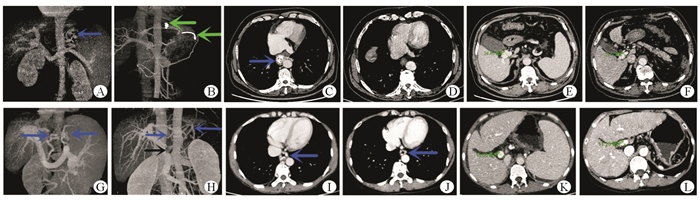
改良组术后3~6个月、1年及至随访截止日食管胃底静脉曲张缓解率为92.68%、87.80%、82.93%,累计1、3、5年再出血率分别为2.78%、12.00%、18.18%;选择组术后3~6个月、1年及至随访截止日食管胃底静脉曲张缓解率为92.86%、87.50%、64.29%,累计1、3、5年再出血率分别为3.85%、21.95%、43.75%。图 4、图 5显示两组患者术前及术后3~6个月胃镜及门静脉系统重建结果。
|
| 图 4 手术前后胃镜所见 A、B:改良组术前食管、胃底黏膜充血,呈红色征,见曲张静脉,略迂曲;C、D:改良组术后3~6个月食管胃底静脉黏膜光滑柔软,吻合口通畅,未见曲张静脉;E、F:选择组术前食管、胃底黏膜稍有充血,见曲张静脉,蛇形迂曲隆起,未见红色征;G、H:选择组术后3~6个月食管、胃底黏膜充血,见曲张静脉,直线型,局部见红色征 |
|
| 图 5 手术前后门静脉系统影像结果 A:CTA示改良组患者术前门脉高压症,食管胃底静脉曲张中、重度;B:CTA示改良组患者术后门脉高压症明显好转,吻合钉、闭合钉在位,吻合口通畅,未见明显食管胃底曲张静脉;C, D:CT示改良组患者术前食管黏膜下曲张静脉明显,管腔狭窄(C),术后曲张静脉消失(D);E, F:CT示改良组患者术前门静脉直径24.40 mm(E),术后门静脉直径13.32 mm(F);G:CTA示选择组患者术前门脉高压症,食管胃底静脉曲张中、重度;H:CTA示选择组术后门脉高压症明显好转,但曲张静脉仍较明显,合并侧支循环形成,且出现门静脉部分栓塞;I, J:CT示选择组患者术前食管黏膜下血管迂曲、隆起(I),术后曲张食管黏膜下静脉曲张仍存在(J);K, L:CT示选择组患者术前门静脉直径15.66 mm(K),术后门静脉直径11.28 mm(L). 蓝色箭头示静脉曲张;绿色箭头示吻合钉、闭合钉;黑色箭头示栓塞 |
结果(表 3)显示:两组术后远期(至随访截止日)累计食管胃底静脉曲张缓解率及再出血率差异有统计学意义(P < 0.05)。两组术后远期门静脉血栓、吻合口狭窄等相关并发症发生率差异均无统计学意义。食管胃底静脉曲张缓解与否、再出血与否及门静脉直径失访10%~15%以多重填补法填补后,两组累计食管胃底静脉曲张缓解率及再出血率差异仍有统计学意义(P < 0.05)。
| 指标 | 改良组(n=41) | 选择组(n=56) | χ2/ t值 | P值 |
| 静脉曲张缓解n(%) | 34(82.93) | 36(64.29) | 4.095 | 0.043 |
| 再出血n(%) | 6(14.63) | 18(32.14) | 3.897 | 0.048 |
| 门静脉直径/mm | 12.02±0.74 | 11.82±0.86 | 1.236 | 0.220 |
| 其他并发症n(%) | ||||
| 门静脉血栓形成 | 11(26.83) | 15(26.79) | 0.028 | 0.868 |
| 顽固性腹水 | 8(19.51) | 12(21.43) | 0.008 | 0.927 |
| 粘连性肠梗阻 | 2(4.88) | 3(5.36) | 0.000 | 1.000 |
| 肝性脑病 | 3(7.32) | 2(3.57) | 0.179 | 0.672 |
| 血液系统疾病 | 2(4.88) | 1(1.79) | 0.105 | 0.745 |
| 吻合口狭窄* | 2(4.88) | 0(0.00) | — | 0.165 |
| 多重填补后随访 | ||||
| 静脉曲张缓解n(%) | 38(84.44) | 42(64.62) | 5.271 | 0.022 |
| 再出血n(%) | 8(17.78) | 25(38.46) | 5.417 | 0.020 |
| 门静脉直径/mm | 12.05±0.76 | 11.82±0.81 | 1.541 | 0.126 |
| *Fisher精确检验 | ||||
以普萘洛尔为代表的药物治疗、内镜下食管曲张静脉套扎与硬化剂注射治疗以及经颈静脉肝内门体分流术等多种治疗方法对门脉高压症EGVB的患者疗效确切,且有低侵袭性[6-7],但远期疗效均不理想,内镜下治疗后反复出血风险达60%[8]。而且,门脉高压导致脾功能亢进,其引起的严重血小板减少可显著增加自发性出血风险[9]。外科手术治疗能针对性减少门脉高压症EGVB患者的再出血,预防和治疗食管胃底静脉曲张,消除腹水,减少其他相关并发症,并提高患者远期生活质量[10-11]。
3.1 两种术式的疗效门脉高压症与肝硬化同时发展,且常伴随全身血流动力学紊乱。本研究中的两种术式均有助于纠正全身血流动力学的紊乱。选择性断流术通过保留胃冠状静脉和食管旁静脉,维持人体的自发性分流,达到既断流又分流的目的;而改良Sugiura术在传统Sugiura术的基础上,省略经胸断流步骤,仅经腹用管状吻合器行食管下段横断吻合,并保留食管旁静脉的完整性,既能彻底断流又能维持自发性分流。两组患者术后,门脉高压症均得到有效缓解,EGVB再发生减少,且并发症发生率低、程度轻。
本研究中,改良Sugiura术患者的术后远期累计出血率及食管胃底静脉曲张缓解率均优于选择性断流术。断流术术后的远期效果依赖于断流的彻底性及防止血管再生。(1)食管下段的静脉解剖结构分为3层,分别为食管旁静脉、黏膜下静脉及浅层静脉。在门脉高压状态下,黏膜下的表皮内血管迂曲、隆起,血流增加,成为门脉高压患者的主要血管破裂出血点。而改良Sugiura术与选择性断流术主要区别在于前者会横断食管,即把黏膜下静脉、浅层静脉进行彻底断流;而且,在吻合处形成的瘢痕组织既能防止食管-胃底间侧支循环的重建,又能延缓新生血管的形成,降低了远期复发出血率。(2)选择组患者术前均有出血史,且重度食管静脉曲张率达到46.15%(30/65),而改良Sugiura组为40.00%(18/45),提示术前重度的食管胃底静脉曲张可能是术后食管胃底静脉曲张合并再出血的高危因素之一。(3)肝硬化患者因肝脏合成凝血因子减少导致凝血酶原时间延长,且多伴有血小板减少,因此不易发生深静脉血栓。但有研究证实,肝硬化状态并不是门静脉血栓的保护性因素[12]。而且脾切除术后门静脉血栓发生率达33.3%[13],一旦血栓累及胃冠状静脉及食管旁静脉,将失去断流术自发性分流的意义。本研究随访中发现约23.64%(26/110)的患者术后发生了门静脉血栓。蒋春晖[14]等随访选择性断流术后6~12个月患者CT血管成像发现,食管旁静脉均基本闭塞,自发性分流消失,且食管胃底静脉断流的不彻底性增加了再出血的可能性。食管胃底静脉断流不彻底可能是本研究中选择组术后远期再出血率较高的原因。
此外,本研究中两组患者术后生存率差异无统计学意义,可能与两组术后死亡原因中肝功能衰竭及肝癌占比较高,而这两种病因与食管胃底静脉曲张及再出血关系不密切有关,但也说明改良Sugiura术较选择性断流术未带来更好的生存获益。
3.2 操作要点(1) 为提高断流彻底性,术中应常规离断迷走神经干,以暴露食管裂孔周围的高位穿支静脉。(2)可不常规行幽门成形术,因幽门成形术会引起胆汁反流,反而加重肝硬化患者门脉高压性胃病的发生[15]。本组患者中28例未行幽门成形术,但术后均未见明显的胃排空障碍。(3)术中应个体化选择大小合适的吻合器,防止撕裂薄弱的食管壁而致术后发生黏膜渗血。(4)术中常规放置营养管不仅能尽早恢复肠内营养,且能防止术后吻合口狭窄导致的进食困难,给予及时的营养支持治疗。
综上所述,与选择性断流术相比,改良Sugiura术延长了手术时间、增加了术中出血量,但未导致更多的术后并发症及更高的死亡率,且术后远期缓解食管胃底静脉曲张及防止再出血的效果较好,能更好地改善门脉高压症EGVB患者的生存质量。因此,对于门脉高压症合并严重食管胃底静脉曲张且有食管胃底静脉出血史的患者,改良Sugiura术是一种更有效且远期获益更明显的手术方式。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
LUIGIANO C, IABICHINO G, JUDICA A, et al. Role of endoscopy in management of gastrointestinal complications of portal hypertension[J]. World J Gastrointest Endosc, 2015, 7(1): 1-12.
[DOI]
|
| [2] |
FRANCHIS R DE, FACULTY B VI. Expanding consensus in portal hypertension: report of the Baveno Ⅵ Consensus Workshop: stratifying risk and individualizing care for portal hypertension[J]. J Hepatol, 2015, 63(3): 743-752.
[DOI]
|
| [3] |
杨连粤. 门静脉高压症外科治疗进展与展望[J]. 中国实用外科杂志, 2020, 40(2): 180-184, 190. YANG L Y. Progress and prospect of surgical treatment for portal hypertension[J]. Chinese Journal of Practical Surgery, 2020, 40(2): 180-184, 190. [CNKI] |
| [4] |
MERCADO M A. Surgical treatment for portal hypertension[J]. Br J Surg, 2015, 102(7): 717-718.
[DOI]
|
| [5] |
ZHANG Y, ZHANG L, WANG M, et al. Selective esophagogastric devascularization in the modified sugiura procedure for patients with cirrhotic hemorrhagic portal hypertension: a randomized controlled trial[J]. Can J Gastroenterol Hepatol, 2020, 2020: 8839098.
|
| [6] |
VILLANUEVA C, ALBILLOS A, BOSCH J, et al. β blockers to prevent decompensation of cirrhosis in patients with clinically significant portal hypertension (PREDESCI): a randomised, double-blind, placebo-controlled, multicentre trial[J]. Lancet, 2019, 393(10181): 1597-1608.
[DOI]
|
| [7] |
TRIPATHI D, STANLEY A J, HAYES P C, et al. U.K. guidelines on the management of variceal haemorrhage in cirrhotic patients[J]. Gut, 2015, 64(11): 1680-1704.
[DOI]
|
| [8] |
BARI K, GARCIA-TSAO G. Treatment of portal hypertension[J]. World J Gastroenterol, 2012, 18(11): 1166-1175.
[DOI]
|
| [9] |
LIN J, LIU Q, LIANG Z, et al. Laparoscopic selective esophagogastric devascularization and splenectomy for patients with cirrhotic portal hypertension[J]. Wideochir Inne Tech Maloinwazyjne, 2019, 14(2): 187-194.
|
| [10] |
HAO X, DAI K, HE Y, et al. Laparoscopic splenectomy via the spleen bed in combination with selective esophagogastric devascularization for patients with cirrhotic portal hypertension: a single-institution experience[J]. Wideochir Inne Tech Maloinwazyjne, 2020, 15(3): 462-468.
|
| [11] |
ZHAO Y J, WANG C F. The therapeutic effect of splenectomy plus selective pericardial devascularization versus conventional pericardial devascularization on portal hypertension in China: a meta-analysis[J]. Oncotarget, 2018, 9(20): 15398-15408.
[DOI]
|
| [12] |
陈淑靖, 朱蕾, 蒋进军. 肝硬化合并静脉血栓栓塞症的临床诊治[J]. 中国临床医学, 2017, 24(1): 60-65. CHEN S J, ZHU L, JIANG J J. The clinical features of venous thromboembolism in patients with cirrhosis[J]. Chinese Journal of Clinical Medicine, 2017, 24(1): 60-65. [DOI] |
| [13] |
KURATA N, OGURA Y, OGISO S, et al. Splenectomy in living donor liver transplantation and risk factors of portal vein thrombosis[J]. Hepatobiliary Pancreat Dis Int, 2019, 18(4): 337-342.
[DOI]
|
| [14] |
蒋春晖, 吴志勇, 徐庆, 等. 选择性贲门周围血管离断术治疗门静脉高压症的临床价值[J]. 现代生物医学进展, 2015, 15(35): 6915-6918. JIANG C H, WU Z Y, XU Q, et al. The therapeutic effect of selective pericardial devascularization on portal hypertension[J]. Progress in Modern Biomedicine, 2015, 15(35): 6915-6918. [CNKI] |
| [15] |
STEWART C L, WILSON L, HAMM A, et al. Is chemical pyloroplasty necessary for minimally invasive esophagectomy?[J]. Ann Surg Oncol, 2017, 24(5): 1414-1418.
[DOI]
|
 2021, Vol. 28
2021, Vol. 28


