2. 武警内蒙古总队医院妇产科, 呼和浩特 010040
2. Department of Gynaecology and Obestetrics, Inner Mongolia General Hospital of the Armed Police, Hohhot 010040, Inner Mongolia, China
正常卵巢功能的建立和维持决定了女性的生殖寿命,若卵巢功能提前衰退,则会严重影响女性的身心健康。早发性卵巢功能不全(premature ovarian insufficiency, POI)是指女性在40岁以前出现卵巢功能减退,主要表现为月经异常(闭经、月经稀发或频发)、促性腺激素水平升高[卵泡刺激素(FSH)>25 U/L]、雌激素水平波动性下降[1]。其在一般人群发病率为1%~3%[2]。近年来,由于受到基因、环境等多种因素的影响,POI的发病率呈上升趋势[3],然而目前尚缺乏对其有效的治疗方法及药物,因此如何对POI患者进行有效的干预和治疗成为亟待解决的问题[4]。构建动物模型进行POI的病因及治疗措施的研究是一种有效的方法。目前有多种构建POI动物模型的方法,化疗药物诱导是其中之一。本研究将不同浓度的顺铂作用于小鼠卵巢,探讨能够引起小鼠POI的最低有效浓度,从而为临床研究提供一种安全、可靠、便捷的模型构建方案。
1 材料与方法 1.1 实验动物选用SPF级雌性C57BL/6小鼠(6~8周)60只,体质量28~30 g,购于上海西普尔-必凯实验动物有限公司,使用许可证编号:SCXK(沪)2013-0016,于21~25℃、相对湿度50%~70%的条件下,饲养于标准塑料笼内,4只/笼。每日光照12 h,自由饮食、饮水,适应性喂养1周后,每日早晨8点进行阴道涂片,连续10 d,将具有正常动情周期的小鼠纳入实验。
1.2 药物、试剂和仪器顺铂为粉剂,20 mg/支,购自海南齐鲁制药。用0.9%NaCl溶液将顺铂分别配制成1 mg/mL、0.75 mg/mL、0.5 mg/mL的工作液,随用随配。伊红染液、苏木精染液、40%甲醛溶液,小鼠性激素ELISA试剂盒[FSH批号:201905;雌激素(E2)批号:201905]购自上海沪峰生物科技有限公司。主要实验仪器:光学显微镜(上海光学仪器厂),赛默飞离心机,海尔超低温冰箱等。
1.3 动物分组及给药方案将C57BL/6小鼠随机分为4组,每组15只(由SPSS 23. 0软件计算得出),每组按照2 mL/kg(0.02 mL/10 g)进行腹腔(小鼠左侧腹股沟上方)给药,连续7 d。小鼠腹腔注射顺铂的半数致死量(LD50)为11.93 mg/kg[5]。参考Lee等[6]的研究,制定给药方案。(1)对照组:腹腔注射0.9%NaCl溶液;(2)剂量1.0组:腹腔注射0.5 mg/mL顺铂工作液(即1 mg/kg);(3)剂量1.5组:腹腔注射0.75 mg/mL顺铂工作液(即1.5 mg/kg);(4)剂量2.0组:腹腔注射1 mg/mL顺铂工作液(即2 mg/kg)。
1.4 取材方法各组于停药后14 d取材。小鼠以0.9%水合氯醛腹腔注射麻醉后,眼眶取血1 mL,然后取双侧卵巢,测量后保存于4%多聚甲醛溶液中备用。
1.5 观察指标 1.5.1 一般状态小鼠的皮肤色泽、饮食、排便及活动情况,每日记录体质量。
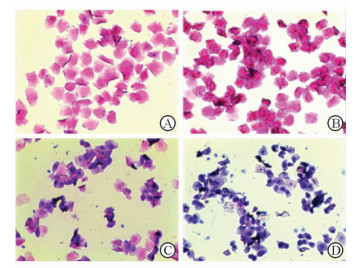
1.5.2 动情周期每日早晨8:00至9:00对小鼠进行阴道脱落细胞(主要为上皮细胞、角化细胞和白细胞)涂片,方法如下:将消毒婴儿棉签用0.9%NaCl溶液湿润后插入小鼠阴道约0.5 cm,顺时针旋转3~4周,抽出棉签,将其上的阴道脱落物旋转涂抹于玻片上(切勿重叠),以4%多聚甲醛固定后进行苏木精-伊红(H-E)染色。光镜下观察细胞形态,判断小鼠动情周期变化。小鼠的正常动情周期一般为4~5 d,分为动情前期、动情期、动情后期和动情间期。各期阴道涂片的特征如下[7]:动情前期为椭圆形有核上皮细胞占大多数,角质化上皮细胞和白细胞很少;动情期为角化上皮细胞占大多数,有核上皮细胞和白细胞很少;动情后期为片状角化上皮细胞、有核上皮细胞和白细胞3种细胞均有,比例无明显差异;动情间期为白细胞占大多数,有核上皮细胞和角质化上皮细胞很少(图 1)。
1.5.3 卵巢组织学形态将以4%多聚甲醛固定后的卵巢进行常规石蜡包埋,制备4 μm切片,H-E染色后,在光镜下计数各类卵泡[8],分别计算卵泡总数、生长卵泡数及闭锁卵泡/卵泡总数比值。
1.5.4 性激素水平将血液标本离心取上清液,采用ELISA法进行小鼠性激素测定。
1.6 统计学处理采用SPSS 23.0软件进行统计分析和描述,对数据进行正态性检验和方差齐性检验;计量资料采用独立样本t检验和单因素方差分析,计数资料采用χ2检验,检验水准(α)为0.05;应用Graphpad Prism 8软件作图。
2 结果 2.1 一般情况除对照组以外,其余各组小鼠从给药第3天开始均出现摄食减少、精神萎靡、消瘦、体毛枯燥黯淡。1.0组程度较轻,停药后迅速恢复;1.5组停药后1周开始好转;2.0组最为严重,持续恶化。给药过程中对照组和1.0组无死亡;1.5组死亡1只(解剖示腹膜积液),死亡率为7%;2.0组死亡4只(解剖示腹膜积液1只,3只原因不明),死亡率为26%。
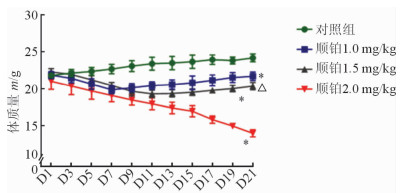
对照组体质量有所增加,而各给药组在给药3 d起均开始减少。1.0组体质量下降较轻,停药后2 d体质量开始回升,停药2周后处死时,体质量基本恢复到给药前水平,平均下降率为1%;1.5组体质量下降较为明显,停药后6 d体质量趋于平稳,停药8 d开始缓慢回升,停药2周后处死时,体质量仍低于给药前,体质量平均下降率为8.5%;2.0组体质量下降最明显,且持续下降,全身状况差,停药2周后处死时,体质量平均下降率为32.6%。各给药组小鼠体质量与对照组差异有统计学意义(P < 0.05),1.5组与2.0组差异有统计学意义(P < 0.05)。结果(图 2)表明,各给药组小鼠体质量均下降,以2.0组体质量下降最明显,对小鼠全身状态影响较大,小鼠死亡数量较多,不利于实验研究。
|
| 图 2 各组小鼠体质量变化曲线 *P < 0.05与对照组比较;△P < 0.05与2.0组比较 |
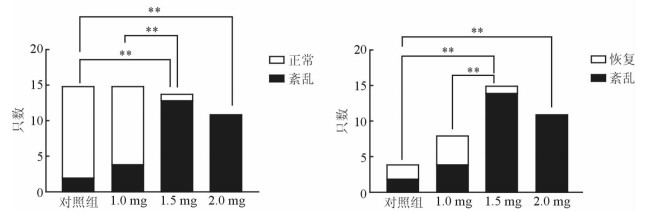
停药后第1天开始进行阴道涂片,判断小鼠动情周期变化情况,直至取材当天。结果(图 3)表明:对照组小鼠动情周期基本正常,仅2只偶发动情周期紊乱,分别表现为动情前期及动情间期延长,均自然恢复,紊乱率为13.3%(2/15),恢复率为100%;1.0组4只出现动情周期紊乱,同样表现为动情后期和动情间期延长,停药7 d后陆续恢复正常,其余11只表现正常,紊乱率为26.7%(4/15),恢复率为100%,与对照组差异无统计学意义;1.5组从停药后第4天陆续出现持续的动情间期或动情后期,停药2周后处死时,仅1只恢复动情周期,紊乱率为100%(14/14),恢复率为7.1%,与对照组差异有统计学意义(P < 0.01),与1.0组差异有统计学意义(P < 0.01);2.0组小鼠阴道干涩,除1只(于第2天开始)外均于停药后第1天出现持续的动情间期,无其余各期出现,停药2周后处死时,均未恢复正常动情期,紊乱率为100%(11/11),恢复率为0%,与对照组差异有统计学意义(P < 0.01),与1.5组差异无统计学意义。
|
| 图 3 各组动物的动情周期紊乱率和紊乱恢复率对比 **P < 0.01 |
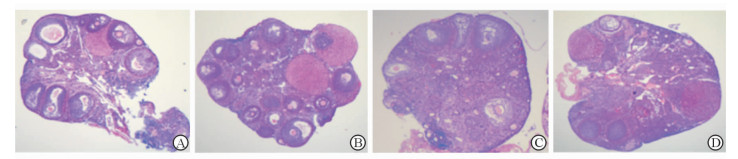
结果(图 4)表明:对照组及1.0组小鼠卵巢表面有多个不规则颗粒状囊泡,颜色红润,各级卵泡(H-E切片)在光镜下清晰可见。1.5组及2.0组小鼠卵巢体积减小,表面无光泽,略发白,颗粒状囊泡明显减少、有不同程度的萎缩;光镜下见卵巢皮质变薄,间质纤维化明显,血管数目减少,各级卵泡明显减少,闭锁卵泡增加,但1.5组可见较为成熟的卵泡,而2.0组几乎没有发育成熟的卵泡。各给药组卵泡总数、生长卵泡数均少于对照组,闭锁卵泡占总卵泡比例均高于对照组,其中1.0组与对照组差异无统计学意义;1.5组及2.0组与对照组差异有统计学意义(P < 0.05);1.5组各项指标与2.0组差异无统计学意义(表 1)。
|
| 图 4 卵巢细胞形态学H-E结果 A:对照组,各级卵泡清晰可见;B:顺铂1.0 mg组各级卵泡可见,结构正常;C:顺铂1.5 mg组,各级卵泡减少,间质纤维化明显,闭锁卵泡数增加,可见较为成熟的卵泡;D:顺铂2.0 mg组,较顺铂1.5 mg组进一步改变,成熟卵泡几乎不可见. Original magnification: ×40 |
| 组别 | 卵泡总数/个 | 生长卵泡/个 | 闭锁卵泡占比 |
| 对照组 | 47.45±3.14 | 45.00±2.36 | 0.05±0.08 |
| 1.0组 | 45.58±3.67 | 42.38±3.15 | 0.07±0.06 |
| 1.5组 | 22.35±4.53* | 12.36±3.36* | 0.44±0.04* |
| 2.0组 | 20.49±3.68* | 9.44±2.96* | 0.54±0.07* |
| *P < 0.05与对照组比较 | |||
各给药组与对照组相比,FSH均上升、E2水平均下降,其中1.0组与对照组差异无统计学意义;1.5组及2.0组与对照组差异有统计学意义(P < 0.05);1.5组与2.0组差异无统计学意义(表 2)。
| 组别 | FSH zB/(U·L-1) | E2 ρB/(ng·L-1) | |||||||||||||||||||||||||||
| 对照组 | 6.44±0.70 | 75.63±5.43 | |||||||||||||||||||||||||||
| 1.0组 | 7.55±0.52 | 70.36±4.22 | |||||||||||||||||||||||||||
| 1.5组 | 12.35±0.96* | 40.38±3.66* | |||||||||||||||||||||||||||
| 2.0组 | 11.35±0.23* | 38.96±2.76* | |||||||||||||||||||||||||||
| FSH:卵泡刺激素;E2:雌二醇. *P < 0.05与对照组比较 | |||||||||||||||||||||||||||||
POI是卵巢早衰(POF)的前驱阶段,如果在此阶段能够实施有效的治疗措施,会使患者避免或延缓POF的发生。建立动物模型是治疗研究的重要前提。
顺铂是治疗妇科恶性肿瘤的一线药物,对卵巢的毒性作用缓和[9],是一种POI动物模型的常用诱导药物[6]。顺铂能够使不同发育阶段的卵泡受到损伤,并且能够抑制卵巢颗粒细胞生长,促进其凋亡,从而使卵泡发育受阻,引起性激素水平变化,最终导致卵巢功能减退[10]。国内外多项研究采用小鼠腹腔连续注射顺铂的方法建立POI的模型,但方案差异较大,且对能够引起小鼠最低有效建模浓度的研究较少。
本实验采用1 mg/kg、1.5 mg/kg、2 mg/kg 3种浓度,连续7 d的给药方式,进行最低建模浓度的研究。结果显示:1.0组小鼠卵巢受损程度较轻,停药后一般状态和动情周期迅速恢复正常,取材时卵巢组织形态、卵泡计数及血清激素水平与对照组相比,变化程度较轻,差异无统计学意义,不能导致小鼠POI的发生,无法用于建模;1.5组小鼠卵巢受损较重,体质量下降平稳,一般状态好,死亡率低,动情周期恢复率低,取材时卵巢组织形态、卵泡计数及血清激素水平与对照组差异均有统计学意义,但变化程度较为平缓,更加符合POI发生的自然变化情况,适宜建立POI模型;2.0组小鼠卵巢受损严重,体质量下降幅度大,全身状况差,耐受性不佳,死亡率高,出现持续的动情间期,取材时卵巢组织形态、卵泡计数及血清激素水平与对照组差异均有统计学意义,但变化剧烈,不利于实验研究。
综上所述,本研究结果显示,1.5 mg/kg为建立C57BL/6小鼠POI模型的合适有效浓度,采用该给药方案建立的模型卵巢组织损伤较为稳定,能够较好地模拟POI患者的激素水平变化,动物耐受性好、死亡率低,代谢功能基本正常,有利于治疗研究的开展,适用于POI治疗方案的评价。
| [1] |
European Society for Human Reproduction and Embryology (ESHRE) Guideline Group on POI, WEBBER L, DAVIES M, et al. ESHRE Guideline:management of women with premature ovarian insufficiency[J]. Hum Reprod, 2016, 31(5): 926-937.
[DOI]
|
| [2] |
KOVANCI E, SCHUTT A K. Premature ovarian failure:clinical presentation and treatment[J]. Obstet Gynecol Clin North Am, 2015, 42(1): 153-161.
[DOI]
|
| [3] |
EBRAHIMI M, AKBARI ASBAGH F. Pathogenesis and causes of premature ovarian failure:an update[J]. Int J Fertil Steril, 2011, 5(2): 54-65.
[URI]
|
| [4] |
QIN Y, JIAO X, SIMPSON J L, et al. Genetics of primary ovarian insufficiency:new developments and opportunities[J]. Hum Reprod Update, 2015, 21(6): 787-808.
[DOI]
|
| [5] |
黄永平, 周世文, 邱磊, 等. 葡萄糖酸锌对小鼠顺铂半数致死量及体内谷胱甘肽含量的影响[J]. 中国医院药学杂志, 1998, 18(2): 55-56. [DOI]
|
| [6] |
LEE E H, HAN S E, PARK M J, et al. Establishment of effective mouse model of premature ovarian failure considering treatment duration of anticancer drugs and natural recovery time[J]. J Menopausal Med, 2018, 24(3): 196-203.
[DOI]
|
| [7] |
李靖, 李炫诚, 吴云霞.确定小鼠动情周期的三种方法[J].实验动物科学, 2007, 24(3): 63-64, 62, 插2. [CNKI]
|
| [8] |
MYERS M, BRITT K L, WREFORD N G, et al. Methods for quantifying follicular numbers within the mouse ovary[J]. Reproduction, 2004, 127(5): 569-580.
[DOI]
|
| [9] |
JAMESDANIEL S, DING D, KERMANY M H, et al. Proteomic analysis of the balance between survival and cell death responses in cisplatin-mediated ototoxicity[J]. J Proteome Res, 2008, 7(8): 3516-3524.
[DOI]
|
| [10] |
SAID R S, MANTAWY E M, EL-DEMERDASH E. Mechanistic perspective of protective effects of resveratrol against cisplatin-induced ovarian injury in rats:emphasis on anti-inflammatory and anti-apoptotic effects[J]. Naunyn Schmiedebergs Arch Pharmacol, 2019, 392(10): 1225-1238.
[DOI]
|
 2020, Vol. 27
2020, Vol. 27