2. 北京大学肿瘤医院核医学科, 北京 100142;
3. 山西医科大学附属第一医院核医学科, 太原 030001;
4. 中山大学附属肿瘤医院核医学科, 广州 510060;
5. 华中科技大学同济医学院附属同济医院核医学科, 武汉 430030;
6. 同济大学附属东方医院核医学科, 上海 200120;
7. 哈尔滨医科大学附属第一医院核医学科, 哈尔滨 150001;
8. 内蒙古医科大学附属医院核医学科, 呼和浩特 010050;
9. 河南省人民医院核医学科, 郑州 450003;
10. 北京协和医院核医学科, 北京 100730;
11. 湖南省肿瘤医院核医学科, 长沙 410013;
12. 河南省人民医院医学影像科, 郑州 450003;
13. 首都医科大学宣武医院核医学科, 北京 100053;
14. 上海联影医疗科技有限公司, 上海 201807;
15. 南京市第一医院核医学科, 南京 210006;
16. 大连医科大学附属第一医院核医学科, 大连 116011;
17. 西南医科大学附属医院核医学科, 泸州 646000;
18. 上海交通大学医学院附属仁济医院, 上海 200127;
19. 山东第一医科大学附属第一医院核医学科, 济南 250014;
20. 梅州市人民医院核医学科, 梅州 514089;
21. 山东第一医科大学附属山东省立医院核医学科, 济南 250021;
22. 南昌医学院第一附属医院江西省人民医院核医学科, 南昌 330006
2. Department of Nuclear Medicine, Peking University Cancer Hospital & Institute, Beijing 100142, China;
3. Department of Nuclear Medicine, First Hospital of Shanxi Medical University, Taiyuan 030001, Shanxi, China;
4. Department of Nuclear Medicine, Sun Yat-sen University Cancer Center, Guangzhou 510060, Guangdong, China;
5. Department of Nuclear Medicine, Tongji Hospital, Tongji Medical College, Huazhong University of Science and Technology, Wuhan 430030, Hubei, China;
6. Department of Nuclear Medicine, Shanghai East Hospital, School of Medicine, Tongji University, Shanghai 200120, China;
7. Department of Nuclear Medicine, First Affiliated Hospital of Harbin Medical University, Harbin 150001, Heilongjiang, China;
8. Department of Nuclear Medicine, Inner Mongolia Medical University Affilated Hospital, Hohhot 010050, Inner Mongolia, China;
9. Department of Nuclear Medicine, Henan Provincial People's Hospital, Zhengzhou 450003, Henan, China;
10. Department of Nuclear Medicine, Peking Union Medical College Hospital, Beijing 100730, China;
11. Department of PET-CT Center, Hunan Cancer Hospital/the Affiliated Cancer Hospital of Xiangya School of Medicine, Central South University, Changsha 410013, Hunan, China;
12. Department of Medical Imaging, Henan Provincial People's Hospital, Zhengzhou 450003, Henan, China;
13. Department of Radiology and Nuclear Medicine, Xuanwu Hospital Capital Medical University, Beijing 100053, China;
14. Shanghai United Imaging Healthcare Co., Ltd., Shanghai 201807, China;
15. Department of Nuclear Medicine, Nanjing First Hospital, Nanjing Medical University, Nanjing 210006, China;
16. Department of Nuclear Medicine, the First Affiliated Hospital of Dalian Medical University, Dalian 116011, Liaoning, China;
17. Department of Nuclear Medicine, Affiliated Hospital of Southwest Medical University, Luzhou 646000, Sichuan, China;
18. Department of Nuclear Medicine, RenJi Hospital, School of Medicine, Shanghai Jiao Tong University, Shanghai 200127, China;
19. Department of Nuclear Medicine, the First Affiliated Hospital of Shandong First Medical University, Jinan 250014, Shandong, China;
20. Department of Nuclear Medicine, Meizhou People's Hospital, Meizhou 514089, Guangdong, China;
21. Department of Nuclear Medicine, Shandong Provincial Hospital Affiliated to Shandong First Medical University, Jinan 250021, Shandong, China;
22. Department of Nuclear Medicine, Jiangxi Provincial People's Hospital, the First Affiliated Hospital of Nanchang Medical College, Nanchang 330006, Jiangxi, China
梗阻性黄疸是临床常见症状之一。其病因为胆管部分或完全阻塞,导致胆汁淤积、肝功能损害和凝血功能障碍等一系列症状,对患者机体造成不同程度的损害[1-2]。病因定位诊断:病变可位于胆道、十二指肠、胰腺等部位;定性诊断:病变分为肿瘤性疾病及非肿瘤性疾病。其中,肿瘤性疾病又包括良性肿瘤(如胆管或十二指肠腺瘤、乳头状瘤、纤维瘤、脂肪瘤等)和恶性肿瘤(如胆管癌、胆囊癌、胰头癌、Vater壶腹癌等);非肿瘤性疾病包括肝内外胆管结石、Mirizzi综合征及胰腺炎、原发性硬化性胆管炎、胆管损伤及胆管先天异常等[1-3]。梗阻性黄疸病因的复杂性给诊断带来挑战。
梗阻性黄疸的影像学检查方法分为有创检查和无创检查。有创检查主要包括内镜逆行胰胆管造影(endoscopic retrograde cholangiopan-creatography,ERCP)、经皮肝穿刺胆管造影(percutaneous transhepatic cholangiography,PTC)及超声内镜。ERCP和PTC对鉴别梗阻性黄疸有重要意义,其优点是诊断准确性高,且在诊断过程中可进行治疗;缺点是当胆道完全梗阻时,ERCP只能显示梗阻点以下的胆道,导致漏诊。PTC适用于肝内胆管扩张或疑似胆总管以上梗阻者。ERCP及PTC均无法获得胆管外病变的信息,定性诊断困难,且作为有创检查,存在胆瘘和出血等并发症发生风险,患者接受程度低[4-5]。超声内镜兼有内镜和超声双重优点,适用于肝内外胆管扩张或合并胰管扩张,且结合细针穿刺能提高远端胆管癌病灶的检出率,尤其适用于难以定位病灶的低位梗阻性黄疸。超声内镜的局限性在于难以发现远处转移,作为侵入性检查技术普及性不高,是非常规检查方法[6-7]。
无创影像学方法包括超声、CT、MRI、PET/CT和PET/MR等。超声能显示肝脏、胆管、胆囊及胰腺的任意断面图像,解剖定位准确,具有较高的普及性和安全性,操作简便、可重复性好,兼有费用低和无辐射等优点,是梗阻性黄疸病因诊断的首选方法;不足之处是易受胃肠道气体干扰,对小病灶或胆总管下段病变显示欠佳,诊断准确性有赖于检查者丰富的经验[5]。增强CT可显示胆管有无梗阻及是否伴占位性病变及其性质,能显示病变范围及其与周围血管的关系,常作为胆管癌、胰腺癌等导致黄疸恶性病变的主要术前评估手段[8];其缺点为有辐射,且对淋巴结转移、远处转移及腹膜种植转移的敏感性欠佳[9]。MR结合胆胰造影(magnetic resonance cholangiopancreatography,MRCP)常用作梗阻性黄疸病因诊断的首选检查方法,部分替代了ERCP和PTC,且无辐射,根据胆胰管“截断”部位对梗阻性黄疸做出定位诊断,根据胆管狭窄区域管壁是否对称、狭窄端是否呈倒杯口状或鸟嘴状等特异性表现作出定性诊断,其诊断准确性优于超声和CT。MRCP结合增强T1W和T2 W可提高梗阻性黄疸病因诊断的准确性,但对远处转移的诊断价值有待提高[10]。
18F-FDG PET/CT是梗阻性黄疸的非首选筛查方法,但在导致梗阻性黄疸的良恶性疾病鉴别诊断及术前评估等方面具有重要价值。Wang等[1]对75例梗阻性黄疸(恶性疾病66例、良性疾病19例)患者的PET/CT影像进行了分析,发现PET/CT对恶性肿瘤导致梗阻性黄疸定性诊断的灵敏度、特异度和准确度分别为86.4%,73.7%和83.5%;结合传统影像方法诊断的灵敏度、特异度和准确度分别为96.5%、57.9%和87.1%。一项对123例胆管癌患者的研究[11]发现,相较于CT检查,PET/CT显像提高了检出局部淋巴结转移(75.9% vs 60.9%)和远处转移(88.3% vs 78.7%)的准确性。
与PET/CT相比,PET/MR兼有MR的高软组织分辨率、MRCP成像及PET分子影像的优势,同时避免了CT辐射。PET/MR诊断腹盆部恶性肿瘤的优势主要体现在对小病灶、淋巴结转移和远处转移的灵敏度高[12-14]。PET与MR多模态影像的优势互补使PET/MR在恶性肿瘤导致梗阻性黄疸的术前诊断与分期、术后随访中发挥重要作用。研究[15]发现,相对于CT、MRI及PET/CT等影像学检查,PET/MR能更精确地评估肝内病变程度,发现或排除远处转移,使29.7%肝内胆管细胞癌患者的治疗决策得以优化。
随着设备的普及和临床应用领域的拓展,PET/MR在梗阻性黄疸的定位和定性诊断方面的价值逐渐显现,但是PET/MR扫描时间长[12],导致患者检查舒适度减低,甚至有部分患者难以配合完成全程检查。在满足诊断需求的前提下,如何缩短扫描时间、选择适宜的个性化扫描协议是临床关注的焦点。基于前期临床探索,使用联影uPMR790 PET/MR的相关专家建立此共识,内容包括PET/MR扫描的适应证与禁忌证、检查前准备、操作规范、PET/MR扫描协议、PET/MR图像解读和报告等。
1 适应证与禁忌证适应证:梗阻性黄疸的病因诊断;引起梗阻性黄疸的恶性肿瘤的术前分期及术后随访。推荐PET/MR成像在有创检查(如PTC、ERCP)前进行[16]。
禁忌证:(1)体内有植入物,包括被动性植入物(如血管夹和金属夹、血管内支架和过滤器、血管通路导管、人工心脏瓣膜、骨科螺钉等植入物及各种人工关节、宫内节育器),主动性植入物(如心脏起搏器和除颤器、耳蜗植入物、电子药物输注泵),其他铁磁性物体或未知物质(颗粒、子弹),需要在检查前仔细询问病史、查阅既往住院病例,并联系植入临床医师或植入物制造商,以获得关于MR安全性和植入物兼容性信息。当患者体内有主动性植入物,但不能明确其在MR环境下的安全性时,严禁对其进行PET/MR检查[17-20]。(2)妊娠及哺乳为PET/MR的相对禁忌[17]。(3)对于患有严重慢性肾脏疾病(肾小球滤过率<30 mL/min)、急性肾损伤的患者和孕妇,禁用钆造影剂进行MR增强检查[17]。
2 检查前准备检查前准备事项:(1)18F-FDG PET/MR检查前,患者禁食4~6 h,检查前24 h内禁止剧烈及长时间运动;(2)注射显像剂后多饮水以减少膀胱辐射剂量[17];(3)如患者带有引流袋,应注意检查有无相关金属部件,同时检查期间避免引流物污染检查床;(4)医师应了解患者使用药物情况,避免所用药物对显像结果造成影响;(5)检查当日家属陪同[21]。
接诊检查医师采集详细病史,核对申请单,确认信息和检查目的,确认患者无检查禁忌证。现场测量身高、体质量和血糖,血糖水平不高于11.1 mmol/L(2 000 mg/L)。
糖尿病患者血糖控制:若检查前血糖偏高,应优先使用口服降糖药,口服降糖药至少4 h后进行PET/MR检查。对于必须使用胰岛素控制血糖的患者,首选速效胰岛素(皮下注射,15 min后进入血液,60 min达峰值,作用持续2~4 h),并在胰岛素注射4 h后注射18F-FDG以进行PET/MR检查。对于使用短效胰岛素(皮下注射,30 min后入血,2~3 h达峰值,作用持续3~6 h)的患者,可在6 h后注射18F-FDG进行PET/MR检查。不推荐糖尿病患者在检查前使用中效胰岛素(作用持续12~18 h)和长效胰岛素(作用持续约24 h)[22]。
3 操作规范放射性药物注射前确认患者信息,按照0.08~0.14 mCi/kg(1 Ci=3.7×1010 Bq)的标准注射18F-FDG。注射18F-FDG后安静休息60 min[23]。
检查前,患者排空小便,更换衣物,移除饰品及随身物品。医师对患者进行呼吸训练,告知患者在呼气末屏气或规律自由呼吸。充分告知患者在检查过程中的噪声及发热情况。使用MR兼容耳机或耳塞进行听力保护。
患者取仰卧位,体中线与检查床中线一致,推荐头先进采集,手臂放在体部两侧并以绑带固定。推荐使用PET/MR兼容的辅助垫固定患者,使其在检查过程中保持体位不变。对于体质瘦弱患者,推荐在生理信号监控气囊上放置一平板垫,保证呼吸信号可被准确采集。使用脊柱线圈和2个体部相控阵线圈进行腹部扫描;正确连接线圈后,在触屏显示面板上确认线圈已被准确识别。体表定位标记为胸骨剑突,使用快速三断面(横断位、冠状位、矢状位)进行定位[21]。
行MR增强扫描时,需提前建立外周静脉通路。不同的对比剂剂量有所不同,注射速率为2~3 mL/s。进行多时相MR增强采集,包括动脉期(注射对比剂后15~20 s)、门静脉期(注射对比剂后60~70 s)和延迟期(注射对比剂后3~5 min)[13, 24]。
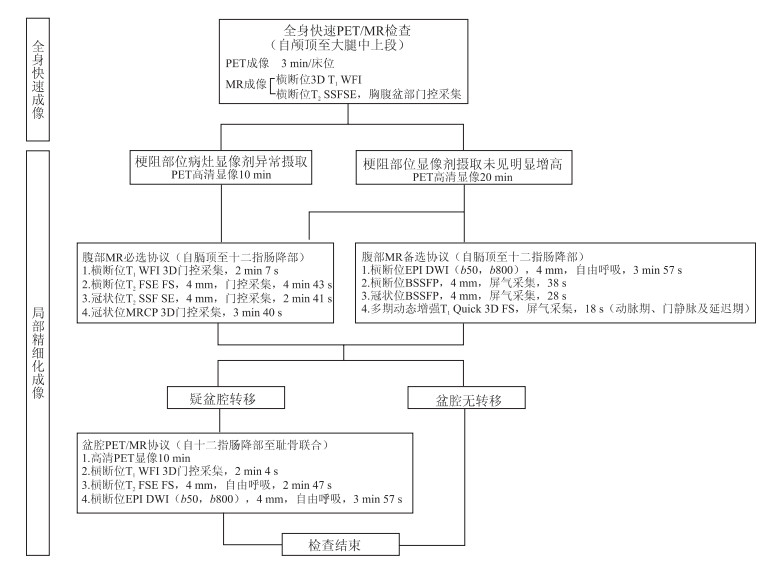
4 PET/MR扫描协议总体原则:基于PET与MR影像的整合优势,在满足诊断需求的前提下,尽可能缩短检查时间。具体方法:基于病灶有无显像剂聚集,建立简繁不同的MRI成像协议,且对所选择的序列按照重要程度依次排序,以最大程度获得具有诊断价值的信息。当病变有显像剂聚集时,通过全身成像信息确定原发灶及需要重点观察的精细扫描范围。此时,PET/MR检查是有选择地借助于MR的多序列和多断面图像,以获得更多梗阻点的形态学信息和病灶毗邻关系的相关信息。当病变无明显显像剂聚集时,须在更大范围内实施MR的多序列和多断面成像,以期获得更多有价值的诊断信息。根据导致梗阻性黄疸病灶对显像剂的不同摄取程度,推荐采用不同的PET/MR扫描协议(图 1)。
|
| 图 1 梗阻性黄疸PET/MR扫描协议优化策略 |
先行自颅顶至大腿中上段的全身快速PET/MR成像,包括横断位T1水脂分离序列(water and fat imaging, WFI)[采用门控采集,以生成磁共振衰减校正图(μ-MAP),同时提供全身3D T1W图像]和横断位T2单次激发快速自旋回波(single-shot fast spin echo,SSFSE)序列(其中胸腹盆部采用门控采集,PET采集时间为3 min/床位,采集参数详见共识[21])。
4.2 上腹部局部精细化成像上腹部扫描范围为自膈顶至十二指肠降部。推荐MR成像使用薄层(4 mm)采集;如患者不能耐受长时间采集,建议选择常规6 mm层厚。T2 W图像采集建议使用ARMS (acquisition correction with radial blade)技术,以减小呼吸运动伪影[25]。PET采集时间为20 min,使用回顾性呼吸门控同步重建(重建比例50%),以消除呼吸位移影响,使PET与MR图像融合精度、对小病灶检测的灵敏度提高。
4.2.1 MR成像必选序列当病灶有显像剂聚集时,下述扫描序列基本可以满足诊断需求。
横断位3D T1WFI:采用Dixon技术,1次成像可获得4组图像(反相位、同相位、脂像和水像),可评估病灶内是否含有脂肪组织。3D MR图像有助于进行横断位、冠状位和矢状位重建。此外,该序列采用门控采集,能与PET图像较好配准,对病灶精确定位具有重要价值。若所采集图像有运动伪影或血管高信号而影响诊断时,加扫T1W 3D快速扰相梯度回波脂肪抑制序列(T1-weighted volume interpolated gradient echo with fat saturation,T1 Quick3D FS),采用屏气采集,但屏气采集图像会影响PET与MRI图像的配准。
横断位T2快速自旋回波抑脂序列(fast spin echo,fat suppression,FSE FS):基于FSE序列的多回波门控触发腹部T2 W脂肪抑制序列,图像分辨率高、对比清晰,能有效发现微小病灶。
冠状位T2 SSFSE门控采集序列:覆盖范围大,可配合横断位图像实现病灶2个方位的定位,对胆道梗阻部位显示较为清楚。
MRCP成像:推荐采用3D门控采集(3~6 min),嘱患者规律自由呼吸,扫描时合理调整定位角度。如需观察肝管结构,扫描模块应与左右肝管走行保持一致;如需观察胆总管及胰管结构,扫描模块应与主胰管走行保持一致。3D MRCP的优势在于信噪比和空间分辨率高,可进行多平面重建,与PET配准精度高,对原始图像进行多角度冠状成像或多层最大密度投影(maximal intensity projection,MIP)重建成像后与PET图像融合,达到最佳的病变显示效果;其不足为延长扫描时间和对运动伪影敏感。若患者呼吸不规律导致3D MRCP图像质量差,可选择2D单激发屏气采集MRCP序列,其特点为成像快,但不能与PET图像配准、融合(图 2)。
|
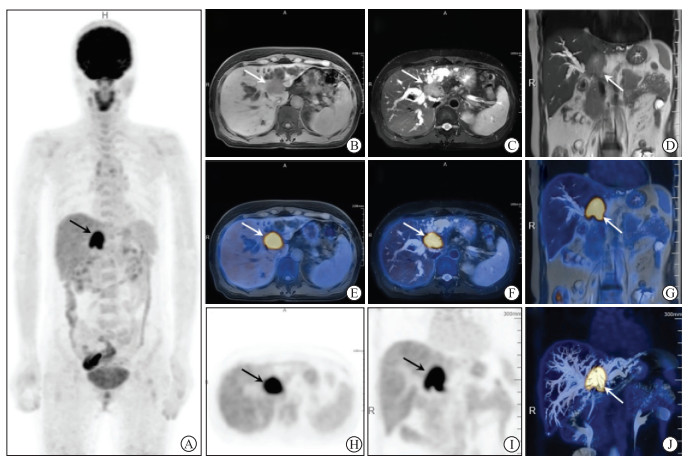
| 图 2 肝门部胆管腺癌(T2 bN0M0)18F-FDG PET/MR图像 患者女性,53岁。A: 全身PET MIP图像,示肝门部糖代谢异常增高灶,其余部位未见明显糖代谢异常增高,肝门部见不规则异常信号肿块;B:横断位T1 WFI水像,呈稍低信号;C: 横断位T2 FSE FS,呈稍高信号;D:冠状位T2 SSFSE MR,呈稍高信号。B~D示病灶与邻近肝脏实质分界欠清,肝内胆管明显扩张。E:横断位T1 WFI水像与PET融合;F:横断位T2 FSE FS与PET融合图像;G:冠状位T2 SSFSE MR与PET融合图像;H、I:横断位(H)及冠状位(I)同层面局部精细化PET图像,示肝门部肿块糖代谢异常增高,大小约为35.5 mm×29.2 mm,最大SUV值约为13.8;J:3D MRCP MIP与PET融合图像,示糖代谢异常增高的肿块位于肝门部胆管,累及左右肝管伴肝内胆管明显扩张,Bismuth-Corlette Ⅳ型。 |
当病灶无明显显像剂聚集时,在上述必选扫描序列的基础上(图 2、3),根据需要增加以下扫描序列。
|
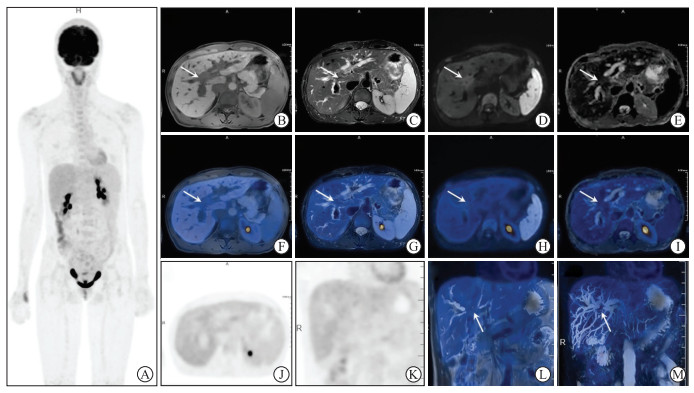
| 图 3 肝门部胆管腺癌(T4N0M0)18F-FDG PET/MR图像 患者女性,47岁。A:全身PET MIP图像,全身未见明显糖代谢异常增高,肝门部胆管壁增厚;B:横断位T1 WFI水像,呈稍低信号;C:横断位T2 FSE FS,呈稍高信号;D:横断位DWI(b=800),呈高信号;E:ADC图像示信号减低,提示弥散受限。B~E示病灶与邻近门静脉右支分界欠清,肝内胆管明显扩张。F:横断位T1 WFI水像与PET融合;G:横断位T2 FSE FS与PET融合图像;H:横断位DWI与PET融合图像;I:横断位ADC与PET融合图像;J:横断位同层面局部精细化扫描PET图像;K、L:冠状位同层面局部精细化扫描PET图像(K)及冠状位T2 SSFSE MR与PET融合图像(L),示肝门部胆管壁增厚,未见明显糖代谢异常增高,大小约为23.1 mm×12.5 mm,最大SUV值约为1.8;M:3D MRCP MIP与PET融合图像,示肝门部胆管充盈缺损,累及左右肝管伴肝内胆管明显扩张,Bismuth-Corlette Ⅳ型,未见糖代谢异常增高。 |
平面回波弥散加权成像(echo-planar imaging diffusion weighted imaging, EPI-DWI; b=50、800):随着硬件和线圈的发展,目前DWI广泛应用于临床肿瘤评估[26-27]。采用自由呼吸采集的薄层DWI序列在梗阻部位病变良恶性鉴别诊断、导致梗阻性黄疸恶性肿瘤的淋巴结转移(图 4)、肝脏转移(图 5)和治疗疗效及随访方面具有一定价值,与高敏感性的PET显像相结合可增加诊断准确性。该序列不足之处为在胃肠道处有明显的形变和异常高信号,与PET配准精度不高。
|
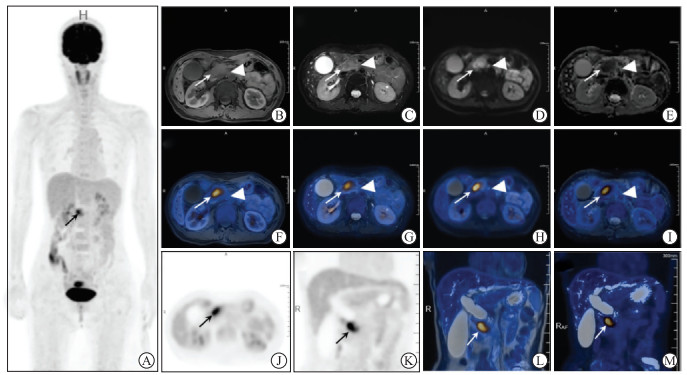
| 图 4 胰头钩突腺癌(T4N1M0)18F-FDG PET/MR图像 患者女性,53岁。A:全身PET MIP,示上腹部近胰头区糖代谢异常增高灶,其余部位未见明显糖代谢异常增高,胰头钩突区见异常信号肿块;B:横断位T1 WFI水像,呈稍低信号;C:横断位T2 FSE FS,呈稍高信号;D:DWI (b=800)呈高信号;E: ADC信号减低;F:横断位T1 WFI水像与PET融合图像;G:横断位T2 FSE FS与PET融合图像;H:横断位DWI与PET融合图像;I:横断位ADC与PET融合图像;J:横断位PET图像;K:冠状位PET图像;L、M:冠状位T2 SSFSE与PET融合图像(L)及3D冠状位MRCP与PET融合图像(M),示胰头钩突区肿块糖代谢异常增高,侵犯胆总管下段及邻近十二指肠降部,大小约为22.0 mm×12.0 mm,最大SUV值约为8.6,胰管及胆总管扩张,呈“双管征”,肝内胆管扩张、胆囊增大。18F-FDG PET/MR图像发现传统影像学没有发现的胰头后方淋巴结转移(三角形),T1 WFI呈稍低信号,T2 FSE FS呈高信号,DWI呈高信号,ADC信号减低,未见明显糖代谢异常增高,大小约为9.5 mm×5.9 mm,最大SUV值约为1.4。 |
|
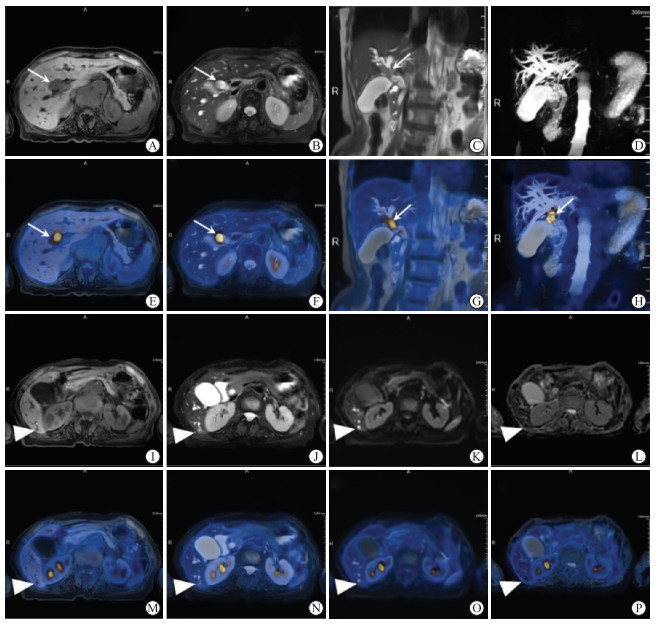
| 图 5 肝门部胆管癌伴肝脏右叶转移18F-FDG PET/MR图像 患者女性,66岁,肝总管及左、右肝管管壁增厚伴糖代谢异常增高,大小约为28.5 mm×17.6 mm,最大SUV值约为14.9。A:横断位T1 WFI水像,呈稍低信号,肝胆管扩张;B:横断位T2 FSE FS,稍高信号;C:冠状位T2 SSFSE,稍高信号;D:3D MRCP MIP,示胆道梗阻部位位于肝门区,累及左、右肝管(Bismuth-Corlette Ⅳ型);E:横断位T1 WFI水像与PET融合图像;F:横断位T2 FSE FS与PET融合图像;G、H:冠状位T2 SSFSE与PET融合图像(G)及3D MRCP MIP与PET融合图像(H)。I~P:肝脏右后叶下段见小圆形异常信号(三角形),代谢略增高。I:横断位T1 WFI水像,异常低信号;J:横断位T2 FSE FS,呈稍高信号;K:DWI(b=800)呈高信号;L:ADC信号减低;M:横断位T1 WFI水像与PET融合图像;N:横断位T2 FSE FS与PET融合图像;O:DWI(b=800)与PET融合图像;P:ADC与PET融合图像,示该病灶糖代谢略增高,直径约为6.4 mm,最大SUV值约为3.6。 |
平衡稳态自由进动序列(balanced steady-state free precession,BSSFP):具有信噪比高、扫描速度快等特征,可显示胆道和血管与毗邻组织关系,结合横断位和冠状位2个方位图像,对梗阻性黄疸的鉴别诊断及有无血管侵犯评价有一定价值,建议扫描层厚4 mm。
4.3 腹盆联合扫描根据全身PET/MR扫描和(或)上腹部扫描所获得的信息,对于疑似有腹盆腔种植转移者,建议行自膈顶至耻骨联合范围内的PET/MR精细成像。盆腔PET采集时间为10 min,选择与该时间相对应的MR采集序列,推荐盆腔成像序列包括T1 WFI、T2 FSE FS及薄层DWI。
4.4 特殊部位局部扫描基于全身PET/MR扫描所获得的信息,对病变或疑似病变部位进行精细化成像,以获得充分的诊断信息。
4.5 动态增强动态增强根据诊断需求作为备选。推荐采用T1 Quick3D FS序列。胆管癌表现为延迟期强化,对导致梗阻性黄疸的病因鉴别诊断有一定价值。值得注意的是,动态增强需要配备高压注射器,并在注射显像剂之前采集所需发射场和T1校准图像用于定量参数的后处理。
5 PET/MR图像解读和报告 5.1 PET/MR图像质量评价重点关注PET计数是否充分,PET与MRI图像配准是否准确,是否存在图像伪影,鉴别PET/MR非操作性原因致运动伪影(包括胃肠道蠕动、血管搏动、呼吸、吞咽所致运动伪影等)以及体内金属或植入物伪影(如胆道植入支架或宫内节育环)。评价采集范围和序列是否满足诊断需求。
5.2 多序列图像对比分析梗阻性黄疸的定位定性诊断需综合T1 WFI、冠状位T2 SSFSE及MRCP多序列的改变进行判断。3D T1 WFI通过低信号的扩张胆管可发现梗阻部位,尤其是横断位、矢状位和冠状位的3D图像易显示梗阻部位形态,与冠状位T2 SSFSE呈高信号的梗阻性扩张的胆管形成对照(图 6),同时能显示病灶与邻近组织之间的关系,较好确定梗阻部位。MRCP能较准确显示胆道梗阻部位、形态和累及范围,但对病变的定性诊断需结合PET显像。如病变部位18F-FDG摄取异常增高,提示病灶生长活跃,对于定位和定性诊断具有指导价值。但部分恶性胆道肿瘤由于含有较多的纤维成分或为管壁浸润性生长类型,在18F-FDG PET显像上表现为低摄取[12-13](图 3)。有胆道介入治疗史或胆道支架植入史的患者由于胆道局部炎症反应,局部18F-FDG摄取异常增高(图 7),不利于病变显示[12-13]。因此,需结合胆道梗阻的形态、T2 WI及DWI等序列进行综合判断。PET/MR显像在胆道有创检查或治疗前进行可提高诊断准确性。此外,MRCP常见的缺陷为显示假性梗阻,如金属物体(夹子、支架)可产生磁敏感相关伪影、空气使图像中局部信号丢失,易与结石或肿瘤混淆,需仔细判别。BSSFP序列对血管病变、静脉血栓或血管侵犯显示较好,在导致梗阻性黄疸恶性肿瘤的可切除性评估中具有参考价值。BSSFP序列不足之处为采用屏气采集,与PET配准不佳;另外,此序列图像上组织信号强度取决于组织的T2 /T1比值,可突出水信号,而其他信号(如肌肉信号)被抑制[28],评估胆道及血管之外的病变时不使用该序列。
|
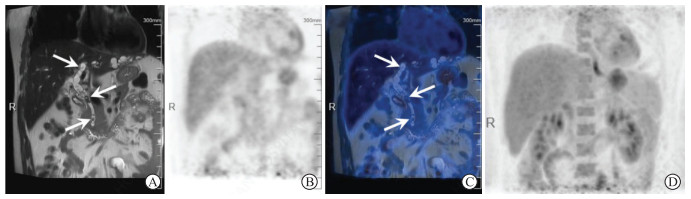
| 图 6 肝内胆管及胆总管多发结石18F-FDG PET/MR图像 患者男性,37岁。A:冠状位T2 SSFSE MR图像,示肝内胆管及胆总管扩张,其内见多发充盈缺损;B:同层面冠状位PET图像,未见明显糖代谢异常增高灶;C:PET与冠状位T2 SSFSE MR融合图像,示肝内胆管及胆总管扩张,其内多发充盈缺损灶未见糖代谢异常增高;D:上腹部PET MIP图像未见糖代谢异常增高灶。箭头示充盈缺损。 |
|
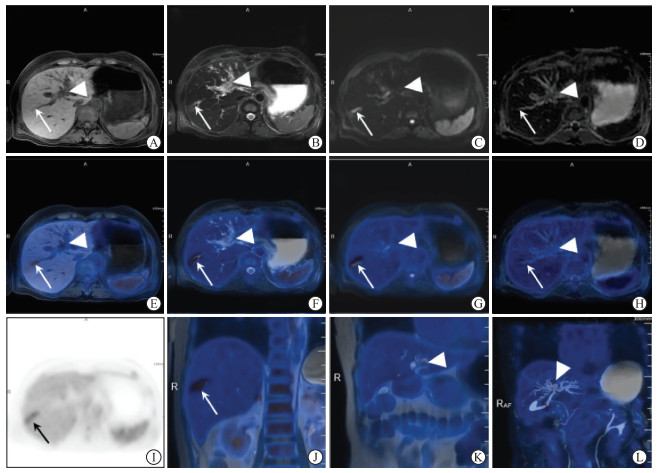
| 图 7 肝门部胆管腺癌(T1N0M0)PTCD术后18F-FDG PET/MR图像 患者女性,61岁,PTCD术后,PET/MR图像示肝脏右叶条状异常信号(箭头)。A:横断位T1 WFI水像,呈稍低信号;B:横断位T2 FSE FS,呈稍高信号;C:横断位DWI(b=800)呈高信号;D:ADC图像,呈稍高信号;E:横断位T1 WFI水像与PET融合;F:横断位T2 FSE FS与PET融合图像;G:横断位DWI与PET融合图像;H:横断位ADC与PET融合图像;I、J:横断位同层面局部精细化扫描PET图像(I)及冠状位T2 SSFSE MR图像与PET融合图像(J),示该处条状糖代谢异常增高,最大SUV值约为4.2,结合病史考虑为PTCD术后炎症。肿瘤位于肝门部肝总管及左右肝管,壁稍增厚(三角形),T1 WFI水像呈稍低信号,T2 FSE FS呈稍高信号,DWI呈稍高信号,ADC信号减低。K:冠状位T2 SSFSE呈稍高信号,未见糖代谢异常增高,最大SUV值约为1.5;L:3D MRCP MIP与PET融合图像,示肝门部胆管充盈缺损,累及左右肝管伴肝内胆管略扩张,Bismuth-Corlette Ⅳ型,未见糖代谢异常增高。 |
一份完整的梗阻性黄疸PET/MR报告应包括检查目的、检查项目、简要病史、报告正文和报告结论[22, 29],各部分内容要点见表 1。
| 项目 | 内容要点 |
| 基本信息 | 姓名、性别、年龄、身高、体质量、来源(门诊或住院)、病案号、检查号 |
| 检查目的 | 病因查找;诊断与分期;疗效评价 |
| 检查项目 | 检查项目及部位,显像剂名称及剂量、注射时间、注射部位,注射后延迟扫描时间及MR扫描协议需在报告描存图中体现 |
| 简要病史 | 主诉,诊疗经过,癌胚抗原(CEA)、糖类抗原199(CA-199)、糖类抗原125(CA-125)等肿瘤标志物,白细胞、中性粒细胞、C反应蛋白等炎症指标,免疫球蛋白G4(IgG4)等免疫指标,US、CT、MR等影像学表现 |
| 报告正文 | 描述各影像所见:(1)使用标准化报告模板,根据解剖区域(如头颈部、胸部、腹部、盆部、骨骼肌肉)的顺序依次描述检查所见;(2)针对病灶的描写应包括病灶定位、数目、大小、形态、边界、范围及与周围组织的关系,病变MR各协议信号变化,显像剂分布是否均匀,病灶PET半定量分析(如最大SUV);(3)针对胆道梗阻的描述应包括梗阻部位、胆道扩张程度、累及范围,MRCP表现;如怀疑肝门胆管癌,需描述Bismuth-Corlette分型;是否伴有胰管扩张;是否伴有显像剂异常摄取,显像剂分布是否均匀,梗阻部位最大SUV等;(4)如疑似胆道恶性肿瘤,需描述有无淋巴结转移及远处脏器转移等;(5)对临床关心问题及部位作针对性描述,包括阴性发现 |
| 报告结论 | (1)诊断明确时给出具体诊断,难于定性者给出倾向性诊断,建议结合具有可操作性的其他检查方法;(2)对于复诊患者,应具有与既往检查结果的对比分析;(3)使用医学术语,避免口语化或易误解的表达,杜绝简单的重复或推诿表达 |
除18F-FDG外,其他放射性示踪剂如镓68(68Ga)四氮杂环十二烷四乙酸-奥曲酸(DOTATATE)长期以来在神经内分泌肿瘤(NET)患者的无创诊断和分期中发挥重要作用[14]。68Ga标记成纤维细胞激活蛋白抑制剂(FAPI)靶向成纤维细胞。成纤维细胞激活蛋白在多种恶性肿瘤中过度表达,包括胆管癌[30]。这些放射性示踪剂在梗阻性黄疸PET/MR显像应用中有一定前景。
利益冲突:所有作者声明不存在利益冲突。
原文发表于《临床癌症通报(英文)》(Clinical Cancer Bulletin)2022年第1卷第2期,详见http://www.clincancerbull.com/en/article/doi/10.11910/j.issn.2791-3937.2022.20220014.
| [1] |
WANG S B, WU H B, WANG Q S, et al. 18F-FDG PET/CT in differentiating malignant from benign origins of obstructive jaundice[J]. Hepatobiliary Pancreat Dis Int, 2015, 14(5): 516-522.
[DOI]
|
| [2] |
PAPADOPOULOS V, FILIPPOU D, MANOLIS E, et al. Haemostasis impairment in patients with obstructive jaundice[J]. J Gastrointestin Liver Dis, 2007, 16(2): 177-186.
|
| [3] |
GROEN P C, GORES G J, LARUSSO N F, et al. Biliary tract cancers[J]. N Engl J Med, 1999, 341(18): 1368-1378.
[DOI]
|
| [4] |
ASGE Standards of Practice Committee, BUXBAUM J L, ABBAS FEHMI S M, SULTAN S, et al. ASGE guideline on the role of endoscopy in the evaluation and management of choledocholithiasis[J]. Gastrointest Endosc, 2019, 89(6): 1075-1105.
[DOI]
|
| [5] |
MODHA K. Clinical approach to patients with obstructive jaundice[J]. Tech Vasc Interv Radiol, 2015, 18(4): 197-200.
[DOI]
|
| [6] |
CHEN C H, TSENG L J, YANG C C, et al. Preoperative evaluation of periampullary tumors by endoscopic sonography, transabdominal sonogrphy and computed tomography[J]. J Clin Ultrasound, 2001, 29(6): 313-321.
[DOI]
|
| [7] |
KHAN S A, DAVIDSON B R, GOLDIN R D, et al. Guidelines for the diagnosis and treatment of cholangiocarcinoma: an update[J]. Gut, 2012, 61(12): 1657-1669.
[DOI]
|
| [8] |
BLECHACZ B. Cholangiocarcinoma: current knowledge and new developments[J]. Gut Liver, 2017, 11(1): 13-26.
[DOI]
|
| [9] |
MARION-AUDIBERT A M, VULLIERME M P, RONOT M, et al. Routine MRI with DWI sequences to detect liver metastases in patients with potentially resectable pancreatic ductal carcinoma and normal liver CT: a prospective multicenter study[J]. AJR Am J Roentgenol, 2018, 211(5): W217-W225.
[DOI]
|
| [10] |
HOEFFEL C, AZIZI L, LEWIN M, et al. Normal and pathologic features of the postoperative biliary tract at 3D MR eholangiopancre-atography and MR imaging[J]. Radiographics, 2006, 26(6): 1603-1620.
[DOI]
|
| [11] |
KIM J Y, KIM M H, LEE T Y, et al. Clinical role of 18F-FDG PET-CT in suspected and potentially operable cholangiocarcinoma: a prospective study compared with conventional imaging[J]. Am J Gastroenterol, 2008, 103(5): 1145-1151.
[DOI]
|
| [12] |
WARD R D, AMORIM B, LI W, et al. Abdominal and pelvic 18F-FDG PET/MR: a review of current and emerging oncologic applications[J]. Abdom Radiol(NY), 2021, 46(3): 1236-1248.
[DOI]
|
| [13] |
GUNIGANTI P, KIERANS A S. PET/MRI of the hepatobiliary system: review of techniques and applications[J]. Clin Imaging, 2021, 71(3): 160-169.
|
| [14] |
GALGANO S J, CALDERONE C E, XIE C, et al. Applications of PET/MRI in abdominopelvic oncology[J]. Radiographics, 2021, 41(6): 1750-1765.
[DOI]
|
| [15] |
FERRONE C, GOYAL L, QADAN M, et al. Management implications of fluorodeoxyglucose positron emission tomography/magnetic resonance in untreated intrahepatic cholangiocarcinoma[J]. Eur J Nucl Med Mol Imaging, 2020, 47(8): 1871-1884.
[DOI]
|
| [16] |
RUYS A T, KATE F J, BUSCH O R, et al. Metastatic lymph nodes in hilar cholangiocarcinoma: does size matter?[J]. HPB (Oxford), 2011, 13(12): 881-886.
[DOI]
|
| [17] |
BRIX G, NEKOLLA E A, NOSSKE D, et al. Risks and safety aspects related to PET/MR examinations[J]. Eur J Nucl Med Mol Imaging, 2009, 36(Suppl 1): S131-S138.
|
| [18] |
TSAI L L, GRANT A K, MORTELE K J, et al. A practical guide to MR imaging safety: what radiologists need to know[J]. Radiographics, 2015, 35(6): 1722-1737.
[DOI]
|
| [19] |
SHELLOCK F G, WOODS T O, CRUES J V 3rd. MR labeling information for implants and devices: explanation of terminology[J]. Radiology, 2009, 253(1): 26-30.
[DOI]
|
| [20] |
GALGANO S, VIETS Z, FOWLER K, et al. Practical considerations for clinical PET/MR imaging[J]. PET Clin, 2018, 13(1): 97-112.
[DOI]
|
| [21] |
陈曙光, 胡鹏程, 樊卫, 等. PET/MR全身显像工作流及协议规划专家共识[J]. 中国临床医学, 2020, 27(4): 713-721. CHEN S G, HU P C, FAN W, et al. Expert consensus on PET/MR whole body imaging workflow and protocol planning[J]. Chin J Clin Med, 2020, 27(4): 713-721. [URI] |
| [22] |
石洪成. PET/CT影像循证解析与操作规范[M]. 上海: 上海科学技术出版社, 2019. SHI H C. PET/CT clinical evidence-based practice and procedure guidance[M]. Shanghai: Shanghai Scientific & Technical Publishers, 2019. |
| [23] |
GAVRA M, SYED R, FRAIOLI F, et al. PET/MRI in the upper abdomen[J]. Semin Nucl Med, 2015, 45(4): 282-292.
[DOI]
|
| [24] |
GANDHI S N, BROWN M A, WONG J G, et al. MR contrast agents for liver imaging: what, when, how[J]. Radiographics, 2006, 26(6): 1621-1636.
[DOI]
|
| [25] |
CHEN S, HU P, GU Y, et al. Impact of patient comfort on diagnostic image quality during PET/MR exam: a quantitative survey study for clinical workflow management[J]. J Appl Clin Med Phys, 2019, 20(7): 184-192.
[DOI]
|
| [26] |
TAOULI B, BEER A J, CHENEVERT T, et al. Diffusion-weighted imaging outside the brain: consensus statement from an ISMRM-sponsored workshop[J]. J Magn Reson Imaging, 2016, 44(3): 521-540.
[DOI]
|
| [27] |
TAOULI B, KOH D M. Diffusion-weighted MR imaging of the liver[J]. Radiology, 2010, 254(1): 47-66.
[DOI]
|
| [28] |
胡鹏程, 赵军, 杨志, 等. 肝胆系统PET/MR成像检查规范专家共识[J]. 中国临床医学, 2020, 27(5): 881-885. HU P C, ZHAO J, YANG Z, et al. Expert consensus on standardization of PET/MR imaging examination of hepatobiliary system[J]. Chin J Clin Med, 2020, 27(5): 881-885. [URI] |
| [29] |
中华医学会核医学分会. PET/MR诊断报告规范化书写专家共识(2020版)[J]. 中华核医学与分子影像杂志, 2020, 40(12): 743-746. Chinese Society of Nuclear Medicine. 2020 Expert consensus for standardized report writing of PET/MR[J]. Chin J Nucl Med Mol Imaging, 2020, 40(12): 743-746. |
| [30] |
KRATOCHWIL C, FLECHSIG P, LINDNER T, et al. 68Ga-FAPI PET/CT: tracer uptake in 28 different kinds of cancer[J]. J Nucl Med, 2019, 60(6): 801-805.
[DOI]
|
 2022, Vol. 29
2022, Vol. 29


