平滑肌肉瘤是一种起源于间质平滑肌细胞的少见肿瘤,占所有软组织肉瘤的15%[1]。下腔静脉平滑肌肉瘤(inferior vena cava leiomyosarcoma, IVCL)早期无典型症状、体征及特异性影像学表现;随着病情进展,大多IVCL向血管腔外生长侵犯肾静脉外侧壁及肾脏,少数也可向腔内生长侵犯下腔静脉及肾静脉内侧壁[2];后期患者可因下腔静脉、肾静脉、肝静脉阻塞及邻近器官受侵犯出现相应症状而就医。
肿瘤完整切除是目前IVCL的首选治疗手段[3]。跨肾静脉开口的IVCL肿瘤大小、位置、生长方式复杂多变,常侵犯整段下腔静脉、单侧或双侧肾静脉、单侧肾脏,手术难度较大。肿瘤完整切除后下腔静脉及肾静脉重建是此类手术的主要难点。本中心提出了“十字三步法”的肿瘤切除及血管重建策略,将手术步骤标准化,并进行了临床实践验证。
1 资料和方法 1.1 一般资料回顾性收集2020年10月至2022年8月接受“十字三步法”手术治疗的9例跨肾静脉开口IVCL患者的临床资料。纳入标准:(1)术前影像学提示肿瘤来源于下腔静脉;(2)肿瘤跨越单侧或双侧肾静脉;(3)首次进行IVCL手术治疗。排除标准:术后病理提示非平滑肌肉瘤。
1.2 术前评估术前完善下腔静脉CTA、肺动脉CTA。通过下腔静脉CTA,对肿瘤的性质作出初步判断,同时明确肿瘤位置、大小、血供、下腔静脉阻塞程度、周围组织器官受累情况(尤其是肾血管受累情况);如肿瘤较大,预计手术难度较大,可行三维重建进一步明确肿瘤与周围组织的关系。通过肺动脉CTA,明确患者术前有无肺栓塞。部分肺栓塞患者临床表现隐匿,术前明确诊断有助于术中及术后评估肺栓塞风险。对于静脉内型IVCL患者,重点评估肺动脉CTA。
1.3 手术方法 1.3.1 肿瘤切除患者取平卧位,接受全身麻醉气管插管。手术采用正中切口,Kocker入路,充分暴露下腔静脉及肿瘤;沿肿瘤外包膜完整游离肿瘤,肿瘤远、近端下腔静脉及双侧肾静脉;下腔静脉上血管阻断带备用,切除下腔静脉肿瘤及受侵犯的脏器,缝合下腔静脉或离断结扎下腔静脉。
1.3.2 “十字三步法”处理血管用带环的聚四氟乙烯(polytetrafluoroethylene, PTFE)人工血管重建肾静脉,用不带环的PTFE人工血管重建下腔静脉。“十字三步法”是一种切除重建策略,旨在分解手术步骤,将复杂的手术过程简单化。“十”:把左右肾静脉看成笔画“横”(一),把下腔静脉看成笔画“竖”(丨)。“三步法”:第1步,完整切除肿瘤,尽可能做到R0切除;第2步,根据“一”(即肾静脉及其侧支损伤情况),确定是否需要进行人工血管重建;第3步,根据“丨”(即下腔静脉缺损情况及侧支循环建立情况),决定是否须进行人工血管重建及方式。
1.4 观察指标观察术后并发症情况,记录联合肾切除的患者术前、术后肾功能指标的变化。采用门诊或电话方式进行随访,随访时间截至2022年9月20日。
1.5 统计学处理采用SPSS 17.0软件进行统计学分析。计数资料以n(%)表示,计量资料以x±s表示;采用配对t检验比较术前、术后血肌酐水平。均为双侧检验,检验水准(α)为0.05。
2 结果 2.1 一般资料9例患者中,男性1例、女性8例,年龄40~69岁,平均(54.0±10.2)岁;肿瘤最大径4.5~17.5 cm,平均(8.2±4.2)cm。生长方式:静脉外型7例,静脉内型1例,混合型1例(肿瘤蔓延至右心房);累及右肾静脉5例,累及左肾静脉3例,累及双肾静脉1例(表 1)。主要临床表现:无明显症状经体检发现者5例,双侧下肢水肿3例,腹痛、腹胀1例;病例5术前已有肝脏多发转移,行姑息性手术治疗。
| 病例 | 性别 | 年龄/岁 | 肿瘤最大径/cm | 肿瘤侵犯 | 手术时间/min | 人工血管重建 | 出血量/mL |
| 1 | 女 | 52 | 12.0 | 下腔静脉、右心房*、左肾静脉 | 190 | 否 | 2 000 |
| 2 | 女 | 44 | 4.5 | 下腔静脉腔内、左肾静脉 | 210 | 否 | 3 500 |
| 3 | 男 | 58 | 6.0 | 下腔静脉、右肾静脉、右肾 | 165 | 否 | 3 500 |
| 4 | 女 | 64 | 8.0 | 下腔静脉、右肾静脉 | 200 | 是 | 3 500 |
| 5 | 女 | 40 | 17.5 | 下腔静脉、左肾静脉 | 165 | 是 | 1 500 |
| 6 | 女 | 42 | 7.0 | 下腔静脉、右肾静脉、右肾、部分十二指肠 | 105 | 否 | 1 000 |
| 7 | 女 | 61 | 6.5 | 下腔静脉、双侧肾静脉 | 260 | 是 | 2 000 |
| 8 | 女 | 56 | 4.5 | 下腔静脉、右肾静脉、部分十二指肠 | 165 | 是 | 400 |
| 9 | 女 | 69 | 7.5 | 下腔静脉、右肾静脉、右肾 | 155 | 是 | 300 |
| *肿瘤达到右心房水平,未侵犯右心房。 | |||||||
所有患者均完成手术并顺利出院,手术时间平均(179.4±42.9)min,手术出血量平均(1 966.7±1 296.1)mL(表 1)。其中,1例静脉内型患者(病例2)术中出现肺栓塞,经积极抢救完成手术。下腔静脉整段切除免重建5例,下腔静脉整段切除人工血管重建1例,下腔静脉部分缺损连续缝合3例;肾静脉人工血管重建4例,其中1例为双侧肾静脉重建;右肾切除3例,左肾切除1例(图 1~2)。

|
| 图 1 9例患者术前肿瘤情况及手术重建方式 A:病例1;B:病例2;C:病例3;D:病例4;E:病例5;F:病例6;G:病例7;H:病例8;I:病例9。 |
|
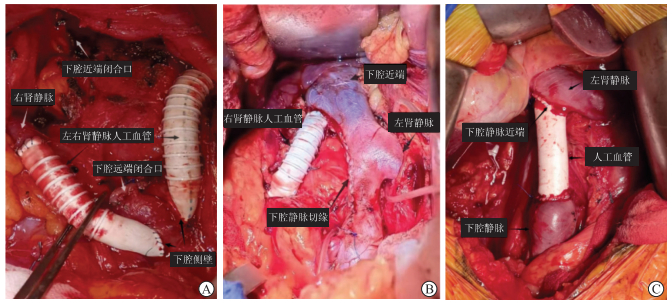
| 图 2 典型病例血管重建 A:病例7,下腔静脉及双侧肾静脉整段切除+双侧肾静脉人工血管重建;B:病例8,右肾静脉切除后人工血管重建、下腔静脉缺损连续缝合;C:病例9,下腔静脉整段切除+人工血管重建。 |
结果(表 2)显示:术前血肌酐平均(81.2±46.8)μmol/L,术后2周血肌酐平均(79.6±32.0)μmol/L,差异无统计学意义。其中,4例单侧肾脏切除患者术前血肌酐平均(76.3±34.5)μmol/L,术后2周血肌酐平均(102.0±35.8)μmol/L,差异无统计学意义;4例术中行肾静脉重建的患者术前血肌酐平均(95.3±62.6)μmol/L,术后2周平均(64.8±13.4)μmol/L,差异无统计学意义。
| 病例 | Cr/(μmol·L-1) | 随访时长/月 | 预后 | |
| 术前 | 术后2周 | |||
| 1 | 45 | 49 | 19 | 术后15个月复发 |
| 2 | 71 | 133 | 18 | 术后4个月复发 |
| 3 | 125 | 133 | 22 | 术后19个月复发 |
| 4 | 189 | 71 | 22 | 术后19个月死亡 |
| 5 | 60 | 50 | 19 | 姑息性手术,带瘤生存 |
| 6 | 65 | 71 | 19 | 术后7个月死亡 |
| 7 | 66 | 80 | 24 | 术后10个月复发 |
| 8 | 66 | 58 | 7 | 未见复发 |
| 9 | 44 | 71 | 2 | 未见复发 |
9例患者术后随访3~22个月。病例3术后出现双下肢水肿,于术后1个月水肿逐渐消退;病例6及病例4分别于术后7个月、19个月死亡;病例2、病例7及病例3分别于术后4个月、10个月及19个月肿瘤复发,带瘤生存,采取靶向药物、免疫治疗、化疗、放疗等综合治疗(表 2)。
3 讨论肿瘤根治性切除术目前是治疗IVCL的金标准[3],完整切除肿瘤可大幅延长患者生存期,1年、3年及5年的总体生存率分别为94%、86%及65%[4]。所谓“十字三步法”,重点在于完整切除肿瘤后下腔静脉及肾静脉的处理。
3.1 “十字三步法”处理下腔静脉下腔静脉部分整段切除后是否需要重建,仍然存在争议。下腔静脉切除后不进行重建,可能导致患者出现术后双下肢水肿;随着手术技术的进步及移植物的研发,部分外科医师建议切除下腔静脉后尽可能进行重建[2, 5-6]。也有学者倾向于下腔静脉切除后免重建,原因为下腔静脉肿瘤一般起病隐匿、病程较长,下腔静脉受压后有充分时间来建立侧支循环;此外,进行血管重建后可能导致严重并发症,如肺栓塞、移植物感染、抗凝药物相关性出血等[7-8]。本中心在临床实践中发现,即使患者术前侧支建立不够充分,术后下肢水肿一般也可在1个月左右逐渐消退,因此大部分病例(如病例1、3~5、7)可免于重建下腔静脉。但当患者病程较短,术前影像学提示下腔静脉通畅,术中下腔静脉断端压力较高时(如病例9),应重建下腔静脉。静脉内型IVCL患者(如病例2)术前、术中均易发生肺栓塞,术前可在近心端放置下腔静脉滤网,术中操作动作要轻柔,挤压肿瘤前应提前在下腔静脉近端阻断,以避免癌栓或血栓脱落导致肺栓塞。下腔静脉缺损较小时(如病例2、6、8),可横向连续缝合静脉壁,修补后管腔直径不应小于正常的1/2;下腔静脉缺损较大时,可采取补片修补。
3.2 “十字三步法”处理肾静脉肾静脉修复重建是保障手术安全性的关键。IVCL手术最常见的并发症为急性肾损伤,发生率约12%;部分患者可进展为尿毒症,须接受长期透析治疗[4]。跨肾静脉开口IVCL切除范围涉及下腔静脉、肾静脉及肾脏,术中应特别注意保护肾静脉的侧支循环,以增加肾静脉免重建的可能性。左肾静脉水平略高于右肾静脉,当肿瘤较大贴近肾静脉时,可采用斜行离断闭合下腔静脉以避免损伤左肾静脉(如病例3、4、9)。右肾静脉粗短并紧贴下腔静脉,下腔静脉肿瘤较易侵犯右肾静脉及右肾,且右肾静脉侧支循环少,部分切除后难以吻合,需要人工血管重建保障血液回流;侵犯右肾时须联合切除右肾(如病例3、6)。而左肾静脉较长,距下腔静脉较远,有左侧生殖静脉、左侧肾上腺静脉、腰静脉等大量侧支血管,当肿瘤仅侵犯左肾静脉开口时,可尝试在左肾静脉与下腔静脉开口处结扎离断左肾静脉,通过速尿法或测压法评估左肾静脉血液回流情况,进而决定是否重建[7];如果术中切除长段左肾静脉或左肾静脉侧支血管被破坏,则须进行人工血管重建。4例肾静脉重建患者术后平均血肌酐水平较术前改善,提示重建有利于肾功能恢复,但有待进一步验证。
肾静脉人工血管吻合方法需根据具体情况而定:一般情况下,下腔静脉部分整段切除闭合后,优先将肾静脉人工血管吻合于下腔静脉近端(如病例5);如术前影像学显示下腔阻塞后大量侧支循环已建立,也可将人工血管吻合于下腔静脉远端(如病例4、7),其优点在于可避免人工血管血栓造成肺栓塞。术后密切监测患者肾功能。人工血管优先吻合于下腔静脉壁,如阻断不便,也可吻合于下腔静脉残端(病例4、5、8)。
综上所述,“十字三步法”作为一种手术策略,可将复杂多变的下腔静脉肿瘤手术步骤进行分解、标准化,具有可复制性,有助于缩短术者学习曲线,手术总体安全可靠,术后患者肾功能恢复良好,亦适用于其他同时侵犯下腔静脉及肾静脉的肿瘤,如巨大肾癌、肾上腺皮质癌等。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
PENEL N, COINDRE J M, GIRAUD A, et al. Presentation and outcome of frequent and rare sarcoma histologic subtypes: a study of 10, 262 patients with localized visceral/soft tissue sarcoma managed in reference centers[J]. Cancer, 2018, 124(6): 1179-1187.
[DOI]
|
| [2] |
KALLURI A G, JAIN A K, RODRIGUEZ H E, et al. Polytetrafluoroethylene is a safe and effective interposition conduit for caval reconstruction after resection of primary leiomyosarcoma of the inferior vena cava[J]. Ann Vasc Surg, 2019, 58: 289-294.
[DOI]
|
| [3] |
DULL B Z, SMITH B, TEFERA G, et al. Surgical management of retroperitoneal leiomyosarcoma arising from the inferior vena cava[J]. J Gastrointest Surg, 2013, 17(12): 2166-2171.
[DOI]
|
| [4] |
NOOROMID M, DE MARTINO R, SQUIZZATO F, et al. Surgical resection and graft replacement for primary inferior vena cava leiomyosarcoma: a multicenter experience[J]. J Vasc Surg Venous Lymphat Disord, 2022, 10(3): 617-625.
[DOI]
|
| [5] |
PANTOJA J L, PATEL R P, BARIL D T, et al. Caval reconstruction with undersized ringed graft after resection of inferior vena cava leiomyosarcoma[J]. Ann Vasc Surg, 2020, 65: 25-32.
[DOI]
|
| [6] |
NOOROMID M J, CAICEDO J C, PHAM D T, et al. Successful resection of a retrohepatic inferior vena cava primary leiomyosarcoma with atrial Thrombus extension in a 30-week pregnant woman[J]. Ann Vasc Surg, 2020, 68: 567.
|
| [7] |
唐茂盛, 苗成利, 陈小兵, 等. 累及下腔静脉腹膜后肿瘤患者行下腔静脉部分整段切除免重建术式的安全性评估[J]. 第二军医大学学报, 2021, 42(6): 693-697. TANG M S, MIAO C L, CHEN X B, et al. Safety of segment resection of inferior vena cava without reconstruction in patients with retroperitoneal tumors[J]. Acad J Second Mil Med Univ, 2021, 42(6): 693-697. [CNKI] |
| [8] |
DAYLAMI R, AMIRI A, GOLDSMITH B, et al. Inferior vena cava leiomyosarcoma: is reconstruction necessary after resection?[J]. J Am Coll Surg, 2010, 210(2): 185-190.
[DOI]
|
 2022, Vol. 29
2022, Vol. 29


