晶体蛋白在晶状体水溶性蛋白中占90%,是哺乳动物晶状体中最主要的成分[1]。晶体蛋白主要分为α、β、γ三大类,分别占40%、35%、25%。其中,α晶体蛋白具有分子伴侣样作用,是一种热休克蛋白,可促进β及γ族晶体蛋白的正确折叠进而形成微观短程有序的结构,并协同促进β及γ族晶体蛋白维持晶状体的正常功能;γ晶体蛋白是晶状体主要结构蛋白,参与晶状体细胞的发育和分化,维持晶状体的透明度[2];β晶体蛋白多为结构蛋白,但同时有某些功能蛋白的特性,尤其是βB2晶体蛋白。
βB2晶体蛋白是β族晶体蛋白族的重要成员,其含量随年龄呈反常依赖性增加,其突变与白内障发生密切相关;该蛋白除在晶状体内高表达外,还高表达于脑组织、视网膜、睾丸及卵巢中[3],参与视神经轴突的再生,影响感觉运动门控和海马功能[4]。此外,本课题组的研究[5]还发现,该蛋白可通过一系列机制影响小鼠的生殖功能。最近有文献[6]报道,βB2晶体蛋白与多种肿瘤的发生、发展相关。本文从这几方面对βB2晶体蛋白的晶状体外功能进行综述。
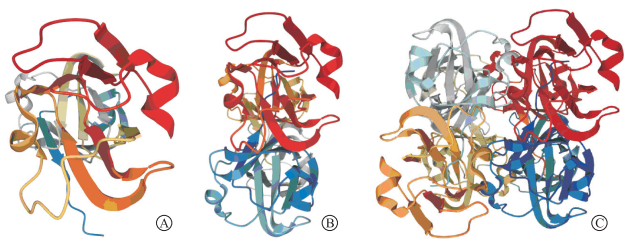
1 βB2晶体蛋白结构特点及表达部位βB2晶体蛋白是晶状体中含量最多的β族晶体蛋白,占晶体蛋白总量的14%~20%。人类βB2晶体蛋白的编码基因(Crybb2;GCID:GC22P025213)在基因组的位置为22q11.23;在小鼠中,Crybb2位于5号染色体。βB2晶体蛋白由205个氨基酸组成,分子量为23 380,等电点为6.54[7]。有研究[8]表明,在人类晶状体中,βB2晶体蛋白是一个结构域交换二聚体;在溶液中,βB2晶体蛋白表现为面对面的二聚体结构。βB2晶体蛋白中存在7个蛋白质区域:4个同源基序、1个连接肽、1个N端延伸和1个C端延伸,其中4个同源基序在βB2晶体蛋白结构域的正确折叠和结构完整性方面有重要作用[9]。这4个基序可与钙离子结合,为钙结合蛋白[10]。其结构特征如图 1所示[11]:
在晶状体中,βB2晶体蛋白定位于晶状体皮质囊膜下,具有很高的溶解性、长期稳定性和抗紫外线损伤的特性[7]。Crybb2基因突变是导致先天性白内障的主要因素[12]。与其他晶状体蛋白相比,βB2晶体蛋白在体内的表达较为特殊:除了晶状体内,其也表达于大脑的不同区域,如海马、嗅球、大脑皮层和小脑[13],以及视网膜、卵巢、睾丸等[3]。本课题组发现,该蛋白在小鼠卵巢中主要表达于颗粒细胞胞浆[5],而在小鼠睾丸中则主要定位于精原细胞[14]。
2 βB2晶体蛋白在晶状体外的表达及功能 2.1 βB2晶体蛋白在视网膜神经节细胞生长及视神经损伤中的作用晶体蛋白可促进离体视网膜神经节细胞(RGC)生长,并促进视神经轴突再生[15]。αB晶体蛋白可抑制RGC膜上钾离子通道kv1.1、kv1.3的表达,使Bcl-xL的表达上升、Caspase-3的表达下降,RGC凋亡减少[16];而由神经祖细胞产生的βB2晶体蛋白则是促进视神经轴突生长的主要晶状体蛋白,向视神经损伤大鼠的玻璃体内注射βB2晶体蛋白可促进大鼠视神经轴突生长[17]。最近的研究[18]发现,视网膜对应于横断和非横断视神经的部分有特定的蛋白质调控,且大多数受调控的蛋白是晶体蛋白家族成员;在大鼠部分视神经横断模型的视网膜上、颞、下、鼻象限4个区域中,βB2晶体蛋白在上、下两个区域表达上调。晶体蛋白的区域诱导能否保护视神经元免受原发性损伤的伤害尚需进一步研究。目前研究采用的βB2晶体蛋白给药方式通常为玻璃体内注射,具有较大的风险,且不易操作,能否通过采用肌肉注射或皮下注射给药而对视神经修复发挥微创、高效的作用有待进一步探讨。
2.2 βB2晶体蛋白在神经系统中的表达及功能过表达Crybb2可促进体外培养海马神经元的树突生长,而下调Crybb2则可抑制树突发生。Crybb2可通过调节Tmsb4X表达介导树突状细胞生长[19],但具体机制有待进一步研究。另外,Crybb2突变对感觉运动门控及海马功能的影响主要表现为前脉冲抑制(PPI)下降、海马体积缩小,同时伴有小白蛋白阳性GABA能中间神经元数量的改变[4]。而PPI降低和小白蛋白阳性中间神经元的改变是精神分裂症的典型内表型,提示Crybb2突变可能与精神分裂症发展相关[20]。Giegling等[21]发现,Crybb2基因突变与抗眼跳功能、工作记忆和视觉记忆能力及感觉运动门控改变有关。但是,目前对于βB2晶状体蛋白影响树突生长的研究多为体外实验,后续须进一步探讨βB2晶状体蛋白在体内对树突生长的影响。由于海马与情绪、学习、记忆等多种功能相关,βB2晶状体蛋白在海马中过表达可能促进学习及记忆功能,但有待研究证实。此外,Crybb2突变与精神分裂的关系,以及该蛋白质或量的变化是否参与影响抑郁症、焦虑症等精神疾病的发生发展均应作为未来研究的方向。
2.3 βB2晶体蛋白在生殖系统中的表达及作用Duprey等[3]研究发现,Crybb2基因突变小鼠生殖功能降低。随后的研究[5, 14]证实,Crybb2基因敲除雌性小鼠卵巢功能下降,动情周期延长,间情期比例升高,21 d内动情周期数显著减少,而Crybb2基因敲除雄性小鼠睾丸中生殖细胞的增殖和凋亡均明显增加,推测Crybb2可能通过Ca2+介导的信号转导机制,影响CaMKⅣ和Bcl-2基因的表达,进而影响生殖。Gao等[22]通过GO数据库及KEGG数据库分析野生型小鼠和基因敲除小鼠睾丸和卵巢中差异表达的lncRNA及mRNA,并用qRT-PCR进行验证,发现lncRNA A-30-P01019163可通过对下游P2rx7 mRNA进行调控,影响睾丸及卵巢组织中细胞的周期及信号转导,从而影响睾丸及卵巢发育。上述研究表明,βB2晶体蛋白缺失或降低会导致小鼠生殖功能降低。但是过表达βB2晶体蛋白能否提高小鼠生殖功能还需要分析。能否根据βB2晶体蛋白与卵巢功能下降的相关性,治疗卵巢早衰及卵巢功能降低患者有待研究。此外,βB2晶体蛋白在体内的正常浓度范围及界定方法也有待明确。Trkova等[23]用超声在两位连续怀孕的孕妇中观察到胎儿双侧白内障畸形,并在用羊水和静脉血提取的DNA中发现了Crybb2的突变。因此,βB2晶体蛋白降低是否与流产相关,流产次数能否影响体内βB2晶体蛋白含量及相关功能,以及βB2晶体蛋白降低与卵子质量及胚胎质量降低之间有无关联等均为进一步研究的方向。
3 βB2晶体蛋白在肿瘤中的表达βB2晶体蛋白与乳腺癌、结直肠癌、前列腺癌、肾细胞癌、胶质母细胞瘤等多种肿瘤密切相关。首先,Crybb2基因在非裔和欧洲裔乳腺癌、结直肠癌、前列腺癌患者体内存在差异表达,其中在非裔美国肿瘤患者体内表达上调,提示Crybb2可作为肿瘤族群差异基因标志[24-27]。另外,Crybb2在非裔肾细胞癌患者体内过表达,且与WNT信号通路相关[28]。在乳腺癌中,Crybb2基因与Crybb2假基因Crybb2P1均与肿瘤生长相关[29]。Crybb2P1基因可通过增强细胞增殖促进肿瘤生长,还可作为非编码RNA调节Crybb2的表达,使其过表达,进而促进肿瘤侵袭、生长、转移及IL-6分泌相关基因的表达,而两者联合过表达可抑制细胞生长[29]。Crybb2在亚裔、非裔及欧洲裔肿瘤患者体内的表达差异有待进一步研究。
4 小结βB2晶体蛋白主要在晶状体内表达,其突变与白内障密切相关。除晶状体外,该蛋白还表达于脑、视网膜、睾丸及卵巢。βB2晶体蛋白可促进轴突和树突生长,在视网膜受损大鼠的玻璃体内注射βB2晶体蛋白可促进视神经生长。其对海马的形态及功能有重要影响。在生殖方面,本课题组[5, 22]发现:首先,βB2晶体蛋白在卵巢及睾丸组织高表达,可能通过Ca2+介导的信号转导机制影响生殖功能,推测Crybb2基因突变可能与之相关。此外,国外研究[24-29]表明,Crybb2过表达或与多种肿瘤发生相关。但是,βB2晶体蛋白的正常范围有待界定。Crybb2基因突变胎儿白内障畸形及流产的相关性,βB2晶体蛋白对精神疾病发病的作用,βB2晶体蛋白在健康人与肿瘤患者以及在不同种族肿瘤患者中的差异表达等有望成为研究热点。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
HEJTMANCIK J F, RIAZUDDIN S A, MCGREAL R, et al. Lens Biology and Biochemistry[J]. Prog Mol Biol Transl Sci, 2015, 134: 169-201.
|
| [2] |
季亚男, 张娟美, 赵友财, 等. 遗传相关的先天性白内障基因突变的研究进展[J]. 国际眼科杂志, 2020, 20(2): 255-257. JI Y N, ZHANG J M, ZHAO Y C, et al. Research progress of genetic related congenital cataract gene mutation[J]. International Eye Science, 2020, 20(2): 255-257. [CNKI] |
| [3] |
DUPREY K M, ROBINSON K M, WANG Y, et al. Subfertility in mice harboring a mutation in betaB2-crystallin[J]. Mol Vis, 2007, 13: 366-373.
|
| [4] |
SUN M X, HÖLTER S M, STEPAN J, et al. Crybb2 coding for βB2-crystallin affects sensorimotor gating and hippocampal function[J]. Mamm Genome, 2013, 24(9-10): 333-348.
[DOI]
|
| [5] |
GAO Q, SUN L L, XIANG F F, et al. Crybb2 deficiency impairs fertility in female mice[J]. Biochem Biophys Res Commun, 2014, 453(1): 37-42.
[DOI]
|
| [6] |
LI M H, LIU S G, HUANG W, et al. Physiological and pathological functions of βB2-crystallins in multiple organs: a systematic review[J]. Aging (Albany NY), 2021, 13(11): 15674-15687.
|
| [7] |
刘鹏, 孙建明. βB2晶体蛋白的功能及相关机制研究进展[J]. 国际检验医学杂志, 2017, 38(4): 505-507. LIU P, SUN J M. Research progress on the function and related mechanism of βB2-crystallin[J]. International Journal of Laboratory Medicine, 2017, 38(4): 505-507. [DOI] |
| [8] |
XI Z Y, WHITLEY M J, GRONENBORN A M. Human βB2-crystallin forms a face-en-face dimer in solution: an integrated NMR and SAXS study[J]. Structure, 2017, 25(3): 496-505.
[DOI]
|
| [9] |
ZHAO W J, XU J, CHEN X J, et al. Effects of cataract-causing mutations W59C and W151C on βB2-crystallin structure, stability and folding[J]. Int J Biol Macromol, 2017, 103: 764-770.
[DOI]
|
| [10] |
JOBBY M K, SHARMA Y. Calcium-binding to lens betaB2-and betaA3-crystallins suggests that all beta-crystallins are calcium-binding proteins[J]. FEBS J, 2007, 274(16): 4135-4147.
[DOI]
|
| [11] |
SMITH M A, BATEMAN O A, JAENICKE R, et al. Mutation of interfaces in domain-swapped human betaB2-crystallin[J]. Protein Sci, 2007, 16(4): 615-625.
[DOI]
|
| [12] |
BELL S, MALKA S, LLOYD I C, et al. Clinical spectrum and genetic diagnosis of 54 consecutive patients aged 0-25 with bilateral cataracts[J]. Genes (Basel), 2021, 12(2): 131.
[DOI]
|
| [13] |
GANGULY K, FAVOR J, NEUHUSER-KLAUS A, et al. Novel allele of Crybb2 in the mouse and its expression in the brain[J]. Invest Ophthalmol Vis Sci, 2008, 49(4): 1533-1541.
[DOI]
|
| [14] |
XIANG F, CUI B, GAO Q, et al. Decreased levels of Ca2+-calmodulin-dependent protein kinase Ⅳ in the testis as a contributing factor to reduced fertility in male Crybb2-/- mice[J]. Int J Mol Med, 2012, 30(5): 1145-1151.
[DOI]
|
| [15] |
王文军, 唐罗生, 杨新光. 不同生长期晶状体蛋白对体外培养的大鼠视网膜神经节细胞存活的促进作用[J]. 西安交通大学学报(医学版), 2011, 32(2): 175-179. WANG W J, TANG L S, YANG X G. Promoting effect of crystallin at different growth stages on the survival of rat retinal ganglion cells in vitro[J]. Journal of Xi'an Jiaotong University (Medical Sciences), 2011, 32(2): 175-179. [CNKI] |
| [16] |
马艳, 吴志鸿, 司南, 等. αB-晶状体蛋白对急性高眼压大鼠视网膜神经节细胞保护作用机制的研究[J]. 眼科新进展, 2015, 35(4): 318-322. MA Y, WU Z H, SI N, et al. Mechanism of αB-crystallin in protecting retinal ganglion cells of rats with acute ocular hypertension[J]. Recent Advances in Ophthalmology, 2015, 35(4): 318-322. [DOI] |
| [17] |
BÖHM M R, PROKOSCH V, BRÜCKNER M, et al. βB2-crystallin promotes axonal regeneration in the injured optic nerve in adult rats[J]. Cell Transplant, 2015, 24(9): 1829-1844.
[DOI]
|
| [18] |
BARROW M A, MARTIN M E, COFFEY A, et al. A functional role for the cancer disparity-linked genes, CRYβB2 and CRYβB2P1, in the promotion of breast cancer[J]. Breast Cancer Res, 2019, 21(1): 105.
[DOI]
|
| [19] |
SUN M, AHMAD N, ZHANG R, et al. Crybb2 associates with Tmsb4X and is crucial for dendrite morphogenesis[J]. Biochem Biophys Res Commun, 2018, 503(1): 123-130.
[DOI]
|
| [20] |
HEERMANN T, GARRETT L, WURST W, et al. Crybb2 mutations consistently affect schizophrenia endophenotypes in mice[J]. Mol Neurobiol, 2019, 56(6): 4215-4230.
[DOI]
|
| [21] |
GIEGLING I, HARTMANN A M, GENIUS J, et al. Polymorphisms in CRYBB2 encoding βB2-crystallin are associated with antisaccade performance and memory function[J]. Transl Psychiatry, 2020, 10(1): 113.
[DOI]
|
| [22] |
GAO Q, REN H, CHEN M, et al. Long non-coding RNAs regulate effects of β-crystallin B2 on mouse ovary development[J]. Mol Med Rep, 2016, 14(5): 4223-4231.
[DOI]
|
| [23] |
TRKOVA M, HYNEK M, DUDAKOVA L, et al. Early detection of bilateral cataracts in utero may represent a manifestation of severe congenital disease[J]. Am J Med Genet A, 2016, 170(7): 1843-1848.
[DOI]
|
| [24] |
WALLACE T A, PRUEITT R L, YI M, et al. Tumor immunobiological differences in prostate cancer between African-American and European-American men[J]. Cancer Res, 2008, 68(3): 927-936.
[DOI]
|
| [25] |
FIELD L A, LOVE B, DEYARMIN B, et al. Identification of differentially expressed genes in breast tumors from African American compared with Caucasian women[J]. Cancer, 2012, 118(5): 1334-1344.
[DOI]
|
| [26] |
D'ARCY M, FLEMING J, ROBINSON W R, et al. Race-associated biological differences among Luminal A breast tumors[J]. Breast Cancer Res Treat, 2015, 152(2): 437-448.
[DOI]
|
| [27] |
JOVOV B, ARAUJO-PEREZ F, SIGEL C S, et al. Differential gene expression between African American and European American colorectal cancer patients[J]. PLoS One, 2012, 7(1): e30168.
[DOI]
|
| [28] |
PAULUCCI D J, SFAKIANOS J P, SKANDERUP A J, et al. Genomic differences between black and white patients implicate a distinct immune response to papillary renal cell carcinoma[J]. Oncotarget, 2017, 8(3): 5196-5205.
[DOI]
|
| [29] |
BARROW M A, MARTIN M E, COFFEY A, et al. A functional role for the cancer disparity-linked genes, CRYβB2 and CRYβB2P1, in the promotion of breast cancer[J]. Breast Cancer Res, 2019, 21(1): 105.
[DOI]
|
 2022, Vol. 29
2022, Vol. 29