临床研究[1]表明,超过半数脑卒中上肢偏瘫患者在发病数月至数年后仍存在上肢功能障碍。因此,脑卒中发生后尽快恢复患者偏瘫上肢运动功能一直是临床康复的重点和难点。神经生理学研究[2]发现,脑卒中发生后健侧对患侧的半球间抑制(inter-hemispheric inhibition, IHI)是影响肢体功能恢复的重要因素。
强制性运动疗法(constraint-induced movement therapy, CIMT)是一种有效改善偏瘫上肢运动功能的新兴康复手段,且有研究[3]表明,CIMT可改善脑卒中后IHI,促进偏瘫肢体运动功能恢复。改良强制性运动疗法(modified constraint-induced movement therapy, mCIMT)源于CIMT,但减弱了对健侧肢体的限制强度,缩短了限制时长,增加了患侧肢体集中训练和密集塑形运动,以保证疗效[4-5]。mCIMT在临床使用中仍有较多制约,难以长期坚持,需要患者及其家属积极配合。因此,在保证mCIMT疗效的前提下如何进一步加快康复进程,缩短治疗周期,成为亟待解决的临床问题。重复经颅磁刺激(repetitive transcranial magnetic stimulation, rTMS)作为非侵入性脑调控技术,可调节大脑皮质兴奋性,改善IHI,促进运动功能恢复[6]。临床上rTMS与多种疗法联用均有良好疗效,为卒中后康复提供了更佳方案[7-9]。目前,mCIMT与rTMS在促进脑卒中患者偏瘫上肢运动功能恢复方面能否发挥协同作用及促进半球间平衡重建,仍需进一步深入研究[10]。
本研究采用mCIMT联合健侧初级运动皮质区(M1区)1 Hz rTMS,观察其对脑卒中患者偏瘫上肢运动功能恢复的影响,同时分析患者神经电生理指标水平,初步探讨其可能的治疗机制。
1 资料与方法 1.1 研究对象选取2020年5月至10月在复旦大学附属金山医院确诊为脑卒中、存在上肢偏瘫并进行康复治疗的患者90例,按随机数字表法随机分为对照组30例、改良组30例和联合组30例。本研究通过复旦大学附属金山医院伦理委员会批准(金医IEC-2020-S43),所有患者均签署知情同意书。
纳入标准:(1)符合第4届全国脑血管疾病学术会议制定的“脑卒中”诊断标准[11],并经头颅MRI或CT检查诊断明确;(2)病程3~6个月,生命体征稳定;(3)18岁≤年龄≤75岁;(4)患侧腕关节可伸展至少20°,除拇指外至少有其他2指掌指关节和指间关节伸展>10°,且动作在1 min内可至少重复3次;(5)患侧上肢改良Ashworth分级≤1+级;(6)可维持静态站姿至少2 min;(7)无认知功能障碍,简易认知状态检查量表(MMSE)≥24分,能配合治疗和评估;(8)签署知情同意书。排除标准:(1)既往有脑卒中病史;(2)佩戴有起搏器、颅内有金属植入物及其他体内金属植入物;(3)颅骨缺损、癫痫,妊娠期、哺乳期或没有采取可靠避孕措施的育龄妇女等;(4)合并严重的心、肺、肝、肾、内分泌和造血系统等疾病者;(5)肢体有明显残缺或其他影响上肢运动的疾病;(6)存在严重认知、言语、视力、听力障碍或精神障碍等影响检查及治疗者;(7)近期参加其他临床试验的患者。
1.2 治疗方法3组患者均接受神经内科药物治疗(如改善循环、营养神经、控制血压等)、日常护理。对照组给予常规康复训练;改良组在常规康复训练基础上增加mCIMT;联合组在常规康复训练基础上给予mCIMT联合健侧M1区1 Hz rTMS。
1.2.1 常规康复训练常规康复训练每次60 min,每天1次,每周5 d,共4周。训练强度应适中,避免引起患者因过度疲劳和不适而影响次日训练。具体内容:(1)良肢位摆放,即患者及其家属进行良肢位摆放的宣教及指导,包括平卧位、侧卧位和坐位姿势调整等;(2)日常生活活动能力训练,即进食、洗脸、如厕、穿衣、刷牙、轮椅操作等训练;(3)患侧肢体被动及主动活动训练;(4)上肢作业疗法。此外,根据患者身体状况适当选择其他辅助性治疗,如气压治疗、电子生物反馈疗法等。
1.2.2 mCIMT法mCIMT法每周进行5 d,持续4周。治疗由两方面组成:一方面,每日使用夹板限制健侧前臂和手部约6 h(含治疗室强化训练2 h);患者自主或在家属督促下完成基本日常动作,包括进食、梳洗、穿衣、开关门等,鼓励患者增加患侧上肢活动时间和强度;在患者参与可能影响自身平衡和安全的活动(如洗澡、如厕)时可解除固定。另一方面,进行上肢强化塑形训练,在训练中选用日常生活常用动作作为塑形动作,包括抓取小球、拿杯子、使用勺子、梳头发、翻书页、插孔练习等,并选择难度略高于患者运动能力的塑形动作。每天在治疗室强化训练2 h,选择3~5种塑形动作,每个动作重复8~10次,剩余时间由家属督促训练,并做好运动日志以便于跟踪反馈。患者取得进步时,治疗师应给予患者明确的反馈性鼓励。随着患者上肢运动能力的恢复,可逐渐增加训练动作的难度和强度,或者减少治疗者的辅助次数。
1.2.3 rTMS采用武汉依瑞德生产的YRD CCY-Ⅰ型经颅磁刺激仪。首先测定每例患者的静息运动阈值(resting motor threshold,RMT):患者取舒适坐位,全身放松,采用“8”字型线圈,线圈与颅骨表面相切,刺激部位选择健侧M1区手功能代表区,采用单脉冲刺激进行RMT测定,以连续刺激10次至少引起5次对侧手背第一骨间背侧肌50 μV运动诱发电位时的最小刺激强度作为该患者的RMT值。刺激方案:患者取仰卧位,佩戴定位帽,采用“8”字型线圈,刺激部位选择健侧M1区,线圈与颅骨表面相切。选择频率1 Hz,刺激强度为80%RMT,每个序列脉冲持续10 s,间歇时间5 s,重复60个序列;持续15 min,共计600个脉冲。经颅磁刺激治疗每天进行1次,每周5 d,共治疗4周。
1.3 评价指标在治疗前和治疗4周后,分别对3组患者进行上肢运动功能评定及神经电生理检测。康复评定采用单盲法,评定医师不参与患者的分组及治疗。
1.3.1 上肢运动功能评定采用Fugl-Meyer上肢运动功能评定量表(Fugl-Meyer assessment scale of upper extremity,FMA-UE)评定上肢运动功能[12],总计33项,每项分3级并依次记为0、1、2分;总分66分,得分越高代表上肢的运动功能越好。
1.3.2 中枢运动传导时间(central motor conduction time,CMCT)治疗前、治疗4周后分别测量CMCT,具体方法:(1)采用经颅磁刺激仪“8”字型线圈,线圈中心位置聚焦大脑卒中侧M1区手功能代表区,给予80%RMT的刺激,在偏瘫侧拇短展肌肌腹位置贴敷电极片,检测运动诱发电位,选取5条波幅较大、重复性较好的波形,记录其潜伏期并计算平均值,所得值为该患者运动诱发电位皮质潜伏期;(2)将“8”字型线圈中心位置对准患者患肢同侧第7颈椎棘突旁,刺激强度为80%RMT,在患侧拇短展肌记录运动诱发电位,选取5条波幅较大、重复性较好的波形,记录其潜伏期并计算平均值,所得值为脊髓潜伏期。CMCT为皮质潜伏期和脊髓潜伏期之差[13]。CMCT可以反映皮质脊髓束(corticospinal tract, CST)通路的功能状态,数值越小表示传导越快,CST功能越好。
1.4统计学处理采用SPSS 19.0统计软件对数据进行分析,采用GraphPad Prism 8软件制作图片。符合正态分布的计量资料以x±s表示,采用方差分析;计数资料以n(%)表示,采用χ2检验。FMA-UE及CMCT采用两因素裂区试验方差分析方法进行分析,若3组间差异显著,则采用Duncan法对其进行两两间比较。检验水准(α)为0.05。
2 结果 2.1 基线资料结果(表 1)显示:3组患者的年龄、性别比例、病程、卒中类型、病变侧等一般资料差异无统计学意义。所有参与本研究的患者均完成了全部试验内容,无中途退出者。所有患者在治疗过程中未发生明显不良反应。
| 指标 | 对照组(n=30) | 改良组(n=30) | 联合组(n=30) | χ2/ F值 | P值 |
| 性别n(%) | 0.378 | 0.828 | |||
| 男 | 20(66.7) | 18(60.0) | 18(60.0) | ||
| 女 | 10(33.3) | 12(40.0) | 12(40.0) | ||
| 年龄/岁 | 56.63±9.57 | 57.47±11.76 | 57.33±12.54 | 0.047 | 0.955 |
| 病程/年 | 125.67±25.02 | 135.60±29.85 | 124.43±21.79 | 1.694 | 0.190 |
| 卒中类型n(%) | 2.105 | 0.349 | |||
| 脑梗死 | 19(63.3) | 24(80.0) | 22(73.3) | ||
| 脑出血 | 11(36.7) | 6(20.0) | 8(26.7) | ||
| 病变侧n(%) | 1.867 | 0.393 | |||
| 左侧 | 17(56.7) | 16(53.3) | 12(40.0) | ||
| 右侧 | 13(43.3) | 14(47.7) | 18(60.0) |
结果(图 1、表 2)显示:FMA-UE评分由治疗前对照组(25.97±5.83)分、改良组(25.47±6.96)分、联合组(26.10±5.29)分,分别提高到治疗后(32.77±7.68)分、(38.07±8.16)分、(42.17±7.89)分。治疗前3组患者FMA-UE评分差异无统计学意义;治疗前后差异有统计学意义(F=684.368, P<0.001);不同干预对FMA-UE影响差异有统计学意义(F=3.799, P=0.026)。两两组间比较显示,治疗后改良组和联合组FMA-UE优于对照组,联合组FMA-UE优于改良组(P<0.05),且组别×时间交互效应差异有统计学意义(F=33.898, P<0.001)。

|
| 图 1 治疗前后3组患者的FMA-UE评分比较 *P < 0.05与对照组相比;△P < 0.05与改良组相比 |
| 评价指标 | 来源 | DF | 离均差平方和 | 均方 | F值 | P值 |
| FMA-UE | 组别 | 2 | 681.64 | 340.82 | 3.799 | 0.026 |
| 时间 | 1 | 6 289.42 | 6 289.42 | 684.368 | < 0.001 | |
| 组别×时间 | 2 | 657.64 | 328.82 | 33.898 | < 0.001 | |
| CMCT | 组别 | 2 | 3.961 | 1.981 | 6.071 | 0.003 |
| 时间 | 1 | 61.484 | 61.484 | 318.266 | < 0.001 | |
| 组别×时间 | 2 | 4.168 | 2.084 | 10.787 | < 0.001 |
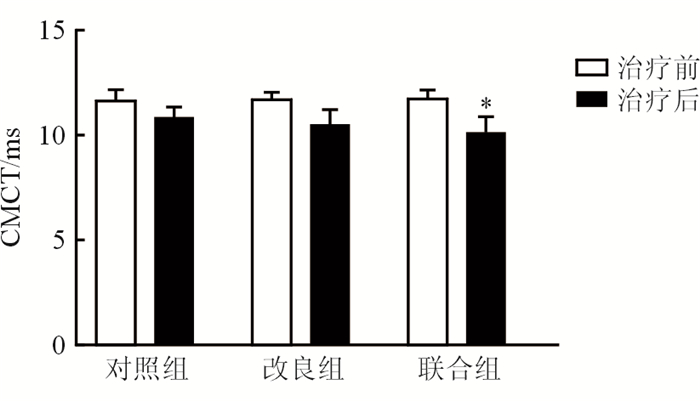
结果(表 2、图 2)显示:CMCT由治疗前对照组(11.78±0.44)ms、改良组(11.62±0.45)ms、联合组(11.78±0.40)ms,缩短到治疗后(10.91±0.44)ms、(10.58±0.60)ms、(10.19±0.67)ms。3组患者治疗前CMCT差异无统计学意义;治疗前后CMCT差异有统计学意义(F=318.266, P<0.001);不同干预对CMCT影响差异有统计学意义(F=6.071, P=0.003)。治疗后两两比较显示,改良组与对照组、改良组与联合组CMCT差异无统计学意义,联合组与对照组差异有统计学意义(P<0.05);且CMCT组别×时间交互效应差异有统计学意义(F=10.787, P<0.001)。
|
| 图 2 治疗前后3组患者CMCT比较 *P < 0.05对照组相比 |
mCIMT源于CIMT,其核心思想是限制健侧肢体,并对患侧肢体进行强化训练,迫使偏瘫肢体进行更多活动,促进其运动功能恢复[14]。临床研究[15-16]表明,mCIMT对脑卒中患者偏瘫肢体功能恢复有良好作用,但其具体机制仍不清楚。Yu等[17]治疗26例脑梗死患者后发现,mCIMT可改善偏瘫上肢运动功能,并提高卒中侧大脑皮层兴奋性。Hu等[18]发现,CIMT可促进卒中大鼠患侧大脑的神经发生和CST结构重塑,促进偏瘫肢体运动功能恢复。这些研究提示mCIMT或CIMT可提高患侧大脑皮层兴奋性,重塑CST功能,从而促进患肢运动功能恢复。
rTMS作为一种非侵入性脑调控技术,可调节大脑皮质兴奋性,改善IHI,促进脑卒中后康复[19]。临床研究[20-22]发现,rTMS对脑卒中后偏瘫上肢运动功能恢复有良好疗效。此外,有研究[23]显示rTMS对皮质下卒中较皮质型卒中更为有效,提示rTMS对脑卒中后CST功能修复有积极作用。
上述研究表明,rTMS和mCIMT均可通过调节大脑兴奋性,改善IHI,重塑CST的功能以促进偏瘫肢体运动功能恢复。由此推测:通过mCIMT提高患侧皮层兴奋性,同时联合健侧M1区1 Hz rTMS抑制健侧皮层兴奋性,可能产生协同作用,进一步提高疗效。
FMA-UE是临床上评价上肢运动功能的主要指标,可较全面反映上肢运动能力。本研究结果显示,经4周治疗后,改良组和联合组患者的FMA-UE评分均优于对照组,差异有统计学意义(P<0.05),且联合组各项指标改善最为显著(P<0.05)。上述结果表明mCIMT或mCIMT联合rTMS对脑卒中患者偏瘫上肢康复均有良好疗效,且联合运用疗效更佳。同时,本研究发现,经4周治疗后,改良组和对照组、改良组和联合组间CMCT差异无统计学意义,联合组和对照组间CMCT差异有统计学意义(P<0.05)。CMCT是评估中枢传导通路功能完整性的神经电生理指标,可反映中枢传导通路功能情况[24]。该结果初步证实,rTMS促进CST功能重塑,mCIMT和rTMS联合应用可能通过改善脑卒中后IHI,产生协同作用。这可能是联合组患者偏瘫上肢运动功能恢复优于其他两组的重要生理基础。
综上所述,本研究结果表明,mCIMT联合健侧M1区1 Hz rTMS可产生协同效应,改善脑卒中后IHI,促进CST功能修复,进而改善偏瘫上肢运动功能。本研究不足之处在于样本量较小,且仅观察了短期疗效,未来将增加样本量,并观察其远期疗效。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
POLLOCK A, FARMER S E, BRADY M C, et al. Interventions for improving upper limb function after stroke[J]. Cochrane Database Syst Rev, 2014, 2014(11): D10820.
[PubMed]
|
| [2] |
CARSON R G. Inter-hemispheric inhibition sculpts the output of neural circuits by co-opting the two cerebral hemispheres[J]. J Physiol, 2020, 598(21): 4781-4802.
[DOI]
|
| [3] |
ABDULLAHI A, TRUIJEN S, SAEYS W. Neurobiology of recovery of motor function after stroke: the central nervous system biomarker effects of constraint-induced movement therapy[J]. Neural Plast, 2020, 2020: 9484298.
|
| [4] |
EL-HELOW M R, ZAMZAM M L, FATHALLA M M, et al. Efficacy of modified constraint-induced movement therapy in acute stroke[J]. Eur J Phys Rehabil Med, 2015, 51(4): 371-379.
[URI]
|
| [5] |
KIM H, YOO E Y, JUNG M Y, et al. The effects of mental practice combined with modified constraint-induced therapy on corticospinal excitability, movement quality, function, and activities of daily living in persons with stroke[J]. Disabil Rehabil, 2018, 40(20): 2449-2457.
[DOI]
|
| [6] |
KLOMJAI W, KATZ R, LACKMY-VALLÉE A. Basic principles of transcranial magnetic stimulation (TMS) and repetitive TMS (rTMS)[J]. Ann Phys Rehabil Med, 2015, 58(4): 208-213.
[DOI]
|
| [7] |
KIM J, YIM J. Effects of high-frequency repetitive transcranial magnetic stimulation combined with task-oriented mirror therapy training on hand rehabilitation of acute stroke patients[J]. Med Sci Monit, 2018, 24: 743-750.
[DOI]
|
| [8] |
JOHNSON N N, CAREY J, EDELMAN B J, et al. Combined rTMS and virtual reality brain-computer interface training for motor recovery after stroke[J]. J Neural Eng, 2018, 15(1): 016009.
[DOI]
|
| [9] |
MILLER K J, GALLINA A, NEVA J L, et al. Effect of repetitive transcranial magnetic stimulation combined with robot-assisted training on wrist muscle activation post-stroke[J]. Clin Neurophysiol, 2019, 130(8): 1271-1279.
[DOI]
|
| [10] |
GILLICK B T, KRACH L E, FEYMA T, et al. Primed low-frequency repetitive transcranial magnetic stimulation and constraint-induced movement therapy in pediatric hemiparesis: a randomized controlled trial[J]. Dev Med Child Neurol, 2014, 56(1): 44-52.
[DOI]
|
| [11] |
中华医学会神经病学分会, 中华医学会神经病学分会脑血管病学组. 中国各类主要脑血管病诊断要点2019[J]. 中华神经科杂志, 2019, 52(9): 710-715. Chinese Society of Neurology, Chinese Stroke Society. Diagnostic criteria of cerebrovascular diseases in China (version 2019)[J]. Chin J Neurol, 2019, 52(9): 710-715. |
| [12] |
HERNÁNDEZ E D, GALEANO C P, BARBOSA N E, et al. Intra- and inter-rater reliability of Fugl-Meyer assessment of upper extremity in stroke[J]. J Rehabil Med, 2019, 51(9): 652-659.
[DOI]
|
| [13] |
TEKGUL H, SAZ U, YILMAZ S, et al. A transcranial magnetic stimulation study for the investigation of corticospinal motor pathways in children with cerebral palsy[J]. J Clin Neurosci, 2020, 78: 153-158.
[DOI]
|
| [14] |
KWAKKEL G, VEERBEEK J M, VAN WEGEN E E, et al. Constraint-induced movement therapy after stroke[J]. Lancet Neurol, 2015, 14(2): 224-234.
[DOI]
|
| [15] |
BALDWIN C R, HARRY A J, POWER L J, et al. Modified Constraint-Induced Movement Therapy is a feasible and potentially useful addition to the Community Rehabilitation tool kit after stroke: a pilot randomised control trial[J]. Aust Occup Ther J, 2018, 65(6): 503-511.
[DOI]
|
| [16] |
DOUSSOULIN A, RIVAS C, RIVAS R, et al. Effects of modified constraint-induced movement therapy in the recovery of upper extremity function affected by a stroke: a single-blind randomized parallel trial-comparing group versus individual intervention[J]. Int J Rehabil Res, 2018, 41(1): 35-40.
[DOI]
|
| [17] |
YU C, WANG W, ZHANG Y, et al. The effects of modified constraint-induced movement therapy in acute subcortical cerebral infarction[J]. Front Hum Neurosci, 2017, 11: 265.
[DOI]
|
| [18] |
HU J, LI C, HUA Y, et al. Constrained-induced movement therapy promotes motor function recovery by enhancing the remodeling of ipsilesional corticospinal tract in rats after stroke[J]. Brain Res, 2019, 1708: 27-35.
[DOI]
|
| [19] |
DIONÍSIO A, DUARTE I C, PATRÍCIO M, et al. The use of repetitive transcranial magnetic stimulation for stroke rehabilitation: a systematic review[J]. J Stroke Cerebrovasc Dis, 2018, 27(1): 1-31.
[DOI]
|
| [20] |
KAKUDA W, ABO M, SASANUMA J, et al. Combination protocol of low-frequency rTMS and intensive occupational therapy for post-stroke upper limb hemiparesis: a 6-year experience of more than 1700 Japanese patients[J]. Transl Stroke Res, 2016, 7(3): 172-179.
[DOI]
|
| [21] |
HIRAKAWA Y, TAKEDA K, TANABE S, et al. Effect of intensive motor training with repetitive transcranial magnetic stimulation on upper limb motor function in chronic post-stroke patients with severe upper limb motor impairment[J]. Top Stroke Rehabil, 2018, 25(5): 321-325.
[URI]
|
| [22] |
VAN LIESHOUT E, VAN DER WORP H B, VISSER-MEILY J, et al. Timing of repetitive transcranial magnetic stimulation onset for upper limb function after stroke: a systematic review and meta-analysis[J]. Front Neurol, 2019, 10: 1269.
[DOI]
|
| [23] |
HSU W Y, CHENG C H, LIAO K K, et al. Effects of repetitive transcranial magnetic stimulation on motor functions in patients with stroke: a meta-analysis[J]. Stroke, 2012, 43(7): 1849-1857.
[DOI]
|
| [24] |
MATSUMOTO H, HANAJIMA R, TERAO Y, et al. Magnetic-motor-root stimulation: review[J]. Clin Neurophysiol, 2013, 124(6): 1055-1067.
[DOI]
|
 2021, Vol. 28
2021, Vol. 28


