肺癌是目前发病率居第2位、死亡率最高的恶性肿瘤[1],其中最常见的是非小细胞肺癌(non-small-cell lung cancer, NSCLC)。约20% NSCLC患者在首次确诊时即已发生纵隔淋巴结的转移[2]。由于早期的随机对照研究[3]未能证明手术组相比于放化疗组的生存优势,对于N2淋巴结阳性患者的治疗,手术价值存在一定的争议。N2患者存在较大的异质性,对于部分T1~2和T3非浸润性的N2患者,新辅助化疗联合手术治疗被广泛认可,并被NCCN指南[4]所推荐。
目前在选择手术对象时,淋巴结转移状态是主要的考虑因素,巨块型N2和多站N2淋巴结转移(N2b)应尽量避免手术。此外,肿瘤大小、手术方式、年龄等一些预后相关因素也常被纳入多因素分析中[5]。对于累及主要支气管或伴有阻塞性肺炎的中央型NSCLC,虽有部分研究[6]表明中央型占位提高了隐匿性N1淋巴结的检出率,但其对N2患者手术预后的影响鲜见报道。本研究旨在通过回顾性分析术后病理证实为N2的NSCLC患者的临床资料,确定中央型占位对N2手术患者预后的影响。
1 资料与方法 1.1 一般资料选择2005年1月1日至2015年12月31日复旦大学附属中山医院胸外科657例接受胸腔镜或开胸根治性手术切除且术后经病理证实为N2淋巴结转移、第8版肺癌TNM分期属于T1~3的NSCLC患者。中央型定义为术后病理证实累及主要支气管或术前影像学资料提示存在阻塞性肺炎。将患者分为中央型组(n=157)和非中央型组(n=500)。患者入院后完善相关术前检查,评估肺功能。所有患者手术后每隔3个月电话随访1次。
纳入标准:(1)接受胸腔镜或开胸根治性手术切除的患者;(2)术后病理证实为NSCLC并伴有N2淋巴结转移;(3)按第8版分期属于T1~3的患者。排除标准:指南未作手术推荐的T4期、浸润性T3期、同一肺叶内伴有恶性结节的T3期患者;伴有远处转移灶或其他手术禁忌证患者。本研究通过复旦大学附属中山医院伦理委员会审批(B2021-128),所有患者均知情并签署知情同意书。
1.2 手术方法全身麻醉后,患者取侧卧位,开胸手术于第5、6肋间做长约15 cm手术切口。胸腔镜手术则于腋中线附近第7、8肋间做1 cm切口,置入胸腔镜为观察孔,腋前线第3、4肋间3 cm切口为主操作孔,肩胛下角线第5、6肋间做2 cm切口为副操作孔。进入胸腔后探查肿瘤位置,游离肿瘤所在肺叶动静脉及支气管,切除肺叶,并进行系统性淋巴结清扫术。创面止血,留置引流管,逐层缝合切口。对于肿瘤累及中央支气管或肺动脉,行肺叶切除无法根治的患者,术中采用游离切断主支气管、肺动脉主干和各肺叶静脉后完成全肺切除。或在能保证切缘干净的情况下,于肿瘤累及的近段切断主支气管、肺动脉干,肿瘤累及的远段切断相邻肺叶的支气管或动脉,再将相邻肺叶的支气管或动脉与主干吻合完成袖式肺叶切除术。对于术前评估肺功能较差无法耐受肺叶切除的外周型结节患者,行局部切除术加淋巴结清扫。
1.3 统计学处理采用SPSS 24.0软件进行数据分析和处理。符合正态分布的计量资料以x±s表示,采用t检验,计数资料以n(%)表示,采用χ2检验。采用Kaplan-Meier法绘制生存曲线描述患者的术后生存情况,采用log-rank检验分析生存曲线差异。采用Cox回归模型分析预后的影响因素。检验水准(α)为0.05。
2 结果 2.1 一般资料分析结果(表 1)显示:中央型组男性患者比例更高(79.0% vs 58.6%),全肺和袖式切除术比例更高(15.3% vs 0.2%, 10.2% vs 1.6%),鳞癌患者更多(57.3% vs 16.6%),肿瘤更大(40.2 mm vs 32.9 mm),累及胸膜的患者比例更低(46.5% vs 65.4%;P < 0.05)。
| 指标 | 合计(n=657) | 中央型组(n=157) | 非中央型组(n=500) | t/ χ2值 | P值 |
| 年龄/岁 | 59.1±10.1 | 60.3±9.4 | 58.7±10.3 | 1.75 | 0.081 |
| 性别n(%) | 21.40 | < 0.001 | |||
| 男 | 417(63.5) | 124(79.0) | 293(58.6) | ||
| 女 | 240(36.5) | 33(21.0) | 207(41.4) | ||
| 手术方式n(%) | 104.10 | < 0.001 | |||
| 肺叶 | 602(91.6) | 117(74.5) | 485(97.0) | ||
| 袖式 | 24(3.7) | 16(10.2) | 8(1.6) | ||
| 全肺 | 25(3.8) | 24(15.3) | 1(0.2) | ||
| 局部切除 | 6(0.9) | 0(0.0) | 6(1.2) | ||
| 病理类型n(%) | 111.00 | < 0.001 | |||
| 腺癌 | 436(66.4) | 52(33.1) | 384(76.8) | ||
| 鳞癌 | 173(26.3) | 90(57.3) | 83(16.6) | ||
| 其他 | 48(7.3) | 15(9.6) | 33(6.6) | ||
| 胸膜侵犯n(%) | 49.00 | 0.022 | |||
| 无 | 157(37.5) | 23(53.5) | 134(35.6) | ||
| 有 | 262(62.5) | 20(46.5) | 242(65.4) | ||
| 分化程度n(%) | 0.10 | 0.738 | |||
| Ⅰ/Ⅱ | 252(38.4) | 62(39.5) | 190(38.0) | ||
| Ⅲ/Ⅳ | 405(61.6) | 95(60.5) | 310(62.0) | ||
| N分期n(%) | 1.10 | 0.294 | |||
| N2a1 | 163(24.8) | 34(21.7) | 129(25.8) | ||
| N2a2/N2b | 494(75.2) | 123(78.3) | 371(74.2) | ||
| 肿瘤最大径/mm | 34.6±13.7 | 40.2±12.9 | 32.9±13.4 | 6.00 | < 0.001 |
| 放化疗 | 2.70 | 0.104 | |||
| 有 | 271(41.2) | 56(35.7) | 215(43.0) | ||
| 无 | 386(58.8) | 101(64.3) | 285(57.0) | ||
| 年龄和直径以x±s表示,其余指标均以n(%)表示 | |||||
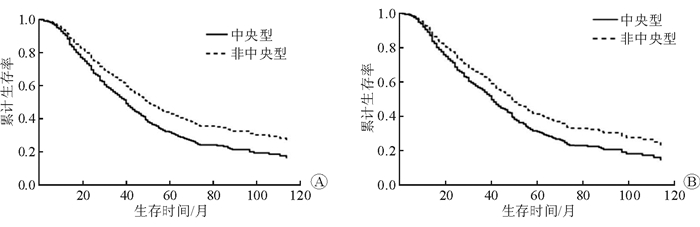
中央型组和非中央型组的中位生存时间分别为30和51个月,5年生存率分别为27.2%和44.8%;Cox多因素分析(图 1A)示两组生存差异存在统计学意义(χ2=19.7,P < 0.001)。结果(表 2)显示:年龄、肿瘤大小、手术方式、N分期、有无放化疗、是否中央型占位是患者手术预后的独立影响因素(P < 0.05)。
|
| 图 1 T1~3 N2(A)和肺叶切除(B)中央型与非中央型患者的生存曲线 |
| 临床因素 | 单因素分析P值 | 多因素分析 | |
| HR(95%CI) | P值 | ||
| 年龄 | < 0.001 | 1.01(1.00~1.03) | 0.011 |
| 肿瘤大小 | 0.013 | 1.01(1.00~1.02) | 0.005 |
| 手术(vs肺叶切除) | 0.015 | < 0.001 | |
| 全肺切除 | 0.713 | 0.54(0.31~0.96) | 0.037 |
| 袖式肺叶切除 | 0.037 | 1.50(0.90~2.53) | 0.123 |
| 局部切除 | 0.015 | 6.84(2.77~16.90) | < 0.001 |
| N (N2a2/N2b vs N2a1) | < 0.001 | 1.98(1.50~2.61) | < 0.001 |
| 放化疗(无vs有) | < 0.001 | 2.89(2.29~3.66) | < 0.001 |
| 中央型(是vs否) | < 0.001 | 1.38(1.06~1.79) | 0.016 |
| 性别(男vs女) | 0.044 | — | 0.163 |
| 病理类型(鳞癌vs腺癌) | < 0.001 | — | 0.451 |
| 胸膜侵犯(有vs无) | 0.110 | — | 0.867 |
| 肿瘤分化(Ⅲ/Ⅳ vs Ⅰ/Ⅱ) | 0.527 | — | 0.972 |
602例接受标准肺叶切除的患者的中位生存期分别为30和51个月,中央型和非中央型的5年生存率分别为27.8%和44.9%;Cox多因素分析(图 1B)示两组差异有统计学意义(χ2=16.9, P < 0.001)。Cox多因素生存分析提示,中央型占位是该类患者手术预后的影响因素(HR=1.34, 95%CI 1.03~1.76, P=0.032)。
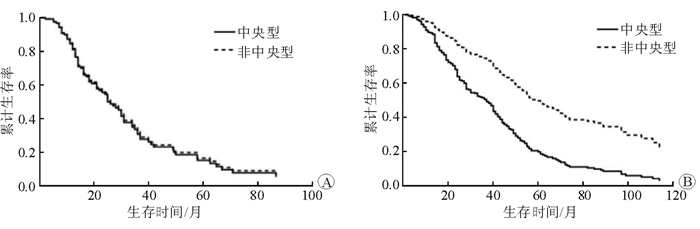
2.3 不同病理类型对患者手术预后的影响602例肺叶切除患者中,鳞癌患者共173例,结果(图3A)显示:中央型与非中央型患者的5年生存率(32.7% vs 36.0%,χ2=0.2, P=0.678)和中位生存期(30个月vs 34个月)差异均无统计学意义,多因素分析也提示中央型不是鳞癌术后预后的影响因素(P=0.899)。
腺癌患者共436例,结果(图3B)显示:中央型与非中央型患者的5年生存率分别为19.4%和48.1%(χ2=16.1, P < 0.001),中位生存期分别为32和56个月(P < 0.05)。多因素分析提示中央型占位为预后相关的独立危险因素(HR=2.30, 95%CI 1.51~3.50,P < 0.001)。
|
| 图 2 鳞癌(A)和腺癌(B)中央型与非中央型患者的生存曲线 |
中央型肺癌的治疗具有一定的挑战性,常因累及中央支气管或动、静脉主干,需行全肺或袖式切除术,伴随较多的围手术期并发症和死亡风险[7]。袖式切除术相比全肺切除术,虽然能更大限度地保留肺功能、改善远期生存[8-9],但手术难度更大,术后发生支气管胸膜瘘等并发症时导致死亡率升高[10]。因病灶靠近纵隔神经及血管等重要结构,给放疗靶区设定也带来一定难度[11],这些都提示中央型肺癌患者可能有更差的预后。但关于中央型占位对手术患者预后的影响,尤其是对N2患者的影响,尚需进一步的研究证明。然而N2患者的综合治疗相对复杂,开展前瞻性随机对照研究也存在一定困难,NCCN指南对于中央型占位给治疗带来的影响并未提出推荐性意见。因此本研究通过回顾性分析N2手术患者的临床资料,结合其他临床因素分析了中央型占位对预后的影响。
在所有N2手术患者中,中央型比非中央型患者的预后显著更差。单因素分析显示,中央型占位与非中央型性别、手术方式、病理类型和肿瘤大小的差异均有统计学意义。男性患者中央型的比例更高,鳞癌比例更高,因此性别与中央型占位之间的关联可能由病理类型引起。虽然有研究[12]表明袖式切除可以获得同肺叶切除类似的生存预后,但多数研究[13-14]仍认为袖式切除也会增加死亡,远期预后变差。本研究中,中央型组包含了更多的袖式和全肺切除术,虽然多因素分析将手术方式也纳入了分析,但为了进一步消除手术方式的影响,本研究筛选接受了标准肺叶切除的患者进行分析。结果依然显示,中央型占位患者较非中央型预后更差,因此中央型肺癌的不良预后可能并非手术方式引起的。本研究中央型肺癌患者的5年总生存率仅为27.2%,在标准肺叶切除组中也仅为27.8%,相比其他研究[15]中ⅢA-N2期手术患者40%左右的5年生存率,预后明显更差,而与报道[16]中ⅢB期20%~30%的生存率更为接近。上述研究表明对于N2患者,即使不行袖式和全肺切除术,中央型也比非中央型患者的预后更差,应当慎重选择。
病理类型可能是影响中央型肺癌患者预后的重要因素,本研究提示中央型肺癌组包含更多的鳞癌患者,虽然鳞癌在单因素分析中相比腺癌具有较差的预后,然而多因素分析显示腺癌和鳞癌患者之间生存差异无统计学意义。随后按照病理类型进行分析发现,鳞癌患者中央型与非中央型之间的生存率差异无统计学意义;而腺癌中央型比非中央型患者的预后明显更差,5年生存率仅19.4%,低于第8版TNM分期中ⅢB期患者的生存率(病理分期26%,临床分期24%),而非中央型的生存率为48.1%。这种较大的差异提示,对于预后较差的中央型N2腺癌患者,应慎重选择手术。有研究[17-18]认为,这种结果可能与中央型肺癌更高的淋巴结转移率相关。本研究中虽然中央型患者中N2a2/N2b的比例比非中央型高(78.3% vs 74.2%),但差异无统计学意义,2组患者阳性淋巴结的数量差异也无统计学意义。此外,N3区域淋巴结因手术不涉及因此无法证明中央型肺癌与N3淋巴结转移相关,关于N2中央型腺癌患者术后预后不良的原因仍有待进一步研究。
综上所述,对于接受手术的N2非小细胞肺癌患者,中央型较非中央型预后更差,中央型是不良预后相关的独立危险因素,且在腺癌患者中更加明显。由于N2中央型腺癌患者术后预后更差,在选择手术时应更加慎重。
利益冲突:所有作者声明不存在利益冲突。
| [1] |
SIEGEL R L, MILLER K D, JEMAL A. Cancer statistics, 2019[J]. CA Cancer J Clin, 2019, 69(1): 7-34.
[DOI]
|
| [2] |
DETTERBECK F C, BOFFA D J, TANOUE L T. The new lung cancer staging system[J]. Chest, 2009, 136(1): 260-271.
[DOI]
|
| [3] |
COUÑAGO F, MONTEMUIÑO S, MARTIN M, et al. Prognostic factors in neoadjuvant treatment followed by surgery in stage ⅢA-N2 non-small cell lung cancer: a multi-institutional study by the Oncologic Group for the Study of Lung Cancer (Spanish Radiation Oncology Society)[J]. Clin Transl Oncol, 2019, 21(6): 735-744.
[DOI]
|
| [4] |
ETTINGER D S, WOOD D E, AGGARWAL C, et al. NCCN guidelines insights: non-small cell lung cancer, version 1.2020[J]. J Natl Compr Canc Netw, 2019, 17(12): 1464-1472.
[DOI]
|
| [5] |
MAO Q, XIA W, DONG G, et al. A nomogram to predict the survival of stage ⅢA-N2 non-small cell lung cancer after surgery[J]. J Thorac Cardiovasc Surg, 2018, 155(4): 1784-1792.
[DOI]
|
| [6] |
DECALUWÉ H, PETERSEN R H, BRUNELLI A, et al. Multicentric evaluation of the impact of central tumour location when comparing rates of N1 upstaging in patients undergoing video-assisted and open surgery for clinical stage Ⅰ non-small-cell lung cancer?[J]. Eur J Cardiothorac Surg, 2018, 53(2): 359-365.
[DOI]
|
| [7] |
KIM A W, BOFFA D J, WANG Z, et al. An analysis, systematic review, and meta-analysis of the perioperative mortality after neoadjuvant therapy and pneumonectomy for non-small cell lung cancer[J]. J Thorac Cardiovasc Surg, 2012, 143(1): 55-63.
[DOI]
|
| [8] |
LANUTI M. Commentary: comparing sleeve lobectomy with pneumonectomy for central lung cancer: a randomized study will never be conducted[J]. J Thorac Cardiovasc Surg, 2020, S0022-5223(20): 32818-X.
|
| [9] |
CHEN J, SOULTANIS K M, SUN F, et al. Outcomes of sleeve lobectomy versus pneumonectomy: a propensity score-matched study[J]. J Thorac Cardiovasc Surg, 2020, S0022-5223(20): 32394-1.
[URI]
|
| [10] |
GRAETER T P. Sleeve lobectomy: perioperative risks and functional results[J]. Chirurg, 2013, 84(6): 469-473.
[DOI]
|
| [11] |
CHANG J Y, BEZJAK A, MORNEX F. Stereotactic ablative radiotherapy for centrally located early stage non-small-cell lung cancer: what we have learned[J]. J Thorac Oncol, 2015, 10(4): 577-585.
[DOI]
|
| [12] |
ZALEPUGAS D, KORYLLOS A, STOELBEN E, et al. Sleeve lobectomy versus lobectomy for primary treatment of non-small-cell lung cancer: a single-center retrospective analysis[J]. J Surg Oncol, 2020, 123(2): 553-559.
|
| [13] |
BERRY M F, WORNI M, WANG X, et al. Sleeve lobectomy for non-small cell lung cancer with N1 nodal disease does not compromise survival[J]. Ann Thorac Surg, 2014, 97(1): 230-235.
[DOI]
|
| [14] |
ABDELSATTAR Z M, SHEN K R, YENDAMURI S, et al. Outcomes after sleeve lung resections versus pneumonectomy in the United States[J]. Ann Thorac Surg, 2017, 104(5): 1656-1664.
[DOI]
|
| [15] |
COLLAUD S, PROVOST B, BESSE B, et al. Should surgery be part of the multimodality treatment for stage ⅢB non-small cell lung cancer?[J]. J Surg Oncol, 2018, 117(7): 1570-1574.
[DOI]
|
| [16] |
DETTERBECK F C, BOFFA D J, KIM A W, et al. The eighth edition lung cancer stage classification[J]. Chest, 2017, 151(1): 193-203.
[DOI]
|
| [17] |
DONG X, QIU X, LIU Q, et al. Endobronchial ultrasound-guided transbronchial needle aspiration in the mediastinal staging of non-small cell lung cancer: a meta-analysis[J]. Ann Thorac Surg, 2013, 96(4): 1502-1507.
[DOI]
|
| [18] |
SCHMIDT-HANSEN M, BALDWIN D R, ZAMORA J. FDG-PET/CT imaging for mediastinal staging in patients with potentially resectable non-small cell lung cancer[J]. JAMA, 2015, 313(14): 1465-1466.
[DOI]
|
 2021, Vol. 28
2021, Vol. 28


